Informacje ogólne
Definicja
- Nowotwory jądra można podzielić na guzy zarodkowe
,(germinalne) i niegerminalne (guzy podścieliskowe-gonadalne, z komórek zrębu inieswoisteguzysznurówz podścieliskapłciowych). - Guz zarodkowy należy do chorób nowotworowych o
Podział na stopnie zaawansowania
- Dostępne są różne systemy klasyfikacji. Najpopularniejsze z
- Klasyfikacja TNM1, która w
- stopnie zaawansowania według klasyfikacji UICC (Union Internationale Contre le Cancer)
- stopień 0: nieinwazyjny nowotwór zarodkowy (GCNIS), N0, M0, S0
- stopień I: brak wykrywalnych przerzutów
IA: pT1, N0, M0, S0
IB: pT2-4, N0, M0, S0
IS: pT1-4, N0, M0, S1-3 - stopień II: przerzuty do węzłów chłonnych zaotrzewnowych poniżej przepony
IIA: pT1-4, N1, M0, S0-1
IIB: pT1-4, N2, M0, S0-1
IIC: pT1-4, N3, M0, S0-1 - stopień III: zaawansowane przerzuty do węzłów chłonnych lub przerzuty odległe
IIIA: pT1-4, N1-3, M1a, S0-1
IIIB: pT1-4, N1-3, M0-1a, S2
IIIC: pT1-4, N1-3, M0-1b, S3
- Klasyfikacja TNM1, która w
- Nowotwory jądra z
- klasyfikacja IGCCCG (International Germ Cell Cancer Collaborative Group)2-4
- podział na dobre, średnie i
- W
Epidemiologia
- U
- Około 95% wszystkich przypadków nowotworu jądra to guzy zarodkowe.
- Około 62% wszystkich guzów zarodkowych to nasieniaki, 1/3 to nienasieniaki.5-6
.
- Około 62% wszystkich guzów zarodkowych to nasieniaki, 1/3 to nienasieniaki.5-6
- Nowotwory gonadalne to najczęściej nowotwory z
guzy ziarnistokomórkoweziarniszczaki.6. - Zapadalność
- Każdego roku na nowotwór jądra zapada 10 na 100
- Każdego roku na nowotwór jądra zapada 10 na 100
- Wiek
- Najczęstszy typ raka u
- Średni wiek zachorowania wynosi 37 lat.
- Najczęstszy typ raka u
- Histologia
- Pacjentami z
.
- Pacjentami z
- Trendy na świecie
- Zapadalność utrzymuje się ostatnio na stałym poziomie po fazie stałego wzrostu obserwowanego od drugiej wojny światowej.
- Czynniki środowiskowe i
- Zapadalność jest najwyższa w
- W Polsce rocznie odnotowuje się około 900 przypadków nowotworu jądra; u 1-3 % pacjentów rozwija się on w obu jądrach.9
Etiologia i patogeneza
- Dokładna przyczyna nie jest znana.
- 95% wszystkich nowotworów jądra powstaje w
. - W
.
Zmiany przedrakowe
- Przypuszcza się, że przyczyną rozwoju nowotworów zarodkowych mogą być komórki rozproszone już w
.,Te rozproszone komktórkire ulegają złośliwemu zwyrodnieniu w
Rak in situ
- U
910. - CIS można też wykryć u
- Jeśli nie zostanie podjęte leczenie, ryzyko przekształcenia się CIS w
. - Rutynowa biopsja jądra przeciwnego nie jest obecnie zalecana. Biopsję można jednak rozważyć u
.
Rak inwazyjny6
- Guzy zarodkowe (germinalne) dzielą się na nasieniaki i
- Czyste nasieniaki stanowią nieco więcej niż połowę wszystkich nowotworów zarodkowych jądra.
- Większość nienasieniaków to guzy mieszane, które zawierają kilka różnych typów komórek, a nasieniak może być jednym z
- Pozostałe typy to raki embrionalne, guzy zatoki endodermalnej, kosmówczaki i
- Jeśli w
- Nowotwory z
gonadalnypodścieliska gonad, komórek zrębowych i sznurów płciowych (niegerminalne)- Do nowotworów gonadalnych zalicza się guzy z
i guzy ziarnistokomórkoweziarniszczaki.
- Do nowotworów gonadalnych zalicza się guzy z
Czynniki predysponujące
- Wnętrostwo
1011 - Nowotwór w
- Istnieje zwiększone ryzyko wystąpienia nowotworu jądra u
1112-1213. - Zwiększone ryzyko zachorowania u
1314. - Zespoły powodujące nieprawidłowy rozwój jąder wydają się być związane ze zwiększonym ryzykiem wystąpienia nowotworów zarodkowych. Zaliczają się do nich np. zespół Downa czy zespół Klinefeltera.
ICD-10
- C62 Nowotwór złośliwy jądra
- C62.0 Jadro niezstąpione
- C62.1 Jądro zstąpione
- C62.9
Diagnostyka
Informacje ogólne
- W
- U
nowo rozpoznanymnoworozpoznanym guzem zarodkowym należy wykonać TK brzucha/miednicy i - RM jamy brzusznej/miednicy należy wykonać w
nowo rozpoznanymnoworozpoznanym guzem zarodkowym, jeśli istnieją przeciwwskazania do podania środka kontrastowego zawierającego jod, takie jak alergia, upośledzona czynność nerek lub zaburzenia czynności tarczycy. Ponadto wwyjaśnieniadiagnostyki zajęcia płuc. - U
dow celu diagnostyki rozsiewu należydodadodatkowo wykonać RM czaszki. - W
- U
przed ablacjąoznaczyć w - Pooperacyjnie u
Kryteria diagnostyczne
- Uwiarygodnienie podejrzenia na podstawie wywiadu lekarskiego i
wynikówwynikubadańbadaniaprzedmiotowychprzedmiotowego- wyczuwalny guz/guzek w
- powiększone jądro
- w
- zwykle brak oznak zakażenia
- ewentualnie ból w
1415
- wyczuwalny guz/guzek w
- Diagnostyka pierwotna obejmuje badanie ultrasonograficzne jąder, którego czułość wynosi niemal 100%.
Diagnostyka różnicowa
- Zapalenie najądrza
- Krwiak lub uraz
- Zapalenie jąder
- Nowotwór jądra może być mylony z
- Jeśli w
- Nowotwór jądra może być mylony z
- Wodniak
- Torbiel nasieniowa
- Skręt jądra
- Naczyniaki wewnątrz- lub zewnątrzjądrowe
1516 - Pierwotny chłoniak jądra (częściej
dotykadotyczy mężczyzn>w wieku >60 lat)1617
Wywiad lekarski
- W
- Czynniki predysponujące
- rak w
- wnętrostwo
- obniżona jakość nasienia/niepłodność
- nowotwór jądra u
1112-1213
- rak w
- Wczesne objawy to często
rozproszonepowiększenie jednego jądra lub twardy guzek, który pacjent wyczuwa w.- Chore jądro nie jest zwykle wrażliwe na dotyk.
- Zazwyczaj pojawia się uczucie ciężkości.
- Ból występuje u
SporadycznieMoże występujepowaćzmniejszonazwiększona tkliwość jądra.- Nieswoiste dolegliwości w
- Pierwszym objawem u
HCGhCG), należy regularnie badać palpacyjnie jądra. - Wodniak występuje u
- 10% pacjentów zgłasza ból pleców.
- Kaszel lub duszność spowodowane przerzutami do pł
ucauc
Badanie przedmiotowe
- Zawsze należy przeprowadzić badanie przedmiotowe moszny.
- Ponadto należy przeprowadzić ogólne badanie przedmiotowe w
.
- Ponadto należy przeprowadzić ogólne badanie przedmiotowe w
- U
rozleglepowiększone jądro lub nieregularnie odgraniczony guz, alezaatakowanechore jądro może być również mniejsze niż normalnie.
Badania uzupełniające w gabinecie lekarza rodzinnego
- Nie
przewidujesąsięwymaganedalszychdalsze działańania.
Diagnostyka specjalistyczna
ProceduryBadania obrazowaniaobrazowe6
UltrasonografiaUSG jądra: najczęściej w- Należy również zbadać ultrasonograficznie jądro przeciwległe w
- Należy również zbadać ultrasonograficznie jądro przeciwległe w
- TK
- klatki piersiowej, jamy brzusznej i
- TK głowy: u
- klatki piersiowej, jamy brzusznej i
- RM
- niestosowany rutynowo
- wykonywany w
- Scyntygrafia kości
- przy odpowiednich objawach
Biomarkery nowotworowe6
- Należy pamiętać, że biomarkery nowotworowe charakteryzują się niską ogólną czułością i
. - Przedoperacyjnie należy zbadać:
- alfafetoproteinę (AFP)
- beta-hCG
- dehydrogenazę mleczanową (LDH)
- AFP i
HCGhCG są podwyższone u
- LDH charakteryzuje się niską swoistością dla nowotworów germinalnych jądra, która
jednakwydaje się nie przekraczać9040-60%w wykrywaniu nawrotów jądra.1718. - Pooperacyjnie należy oznaczyć następujące biomarkery:
- AFP,
- Okres półtrwania AFP i
- Jeśli wartości pozostają podwyższone lub wzrastają po orchiektomii, należy szukać przerzutów.
- Pooperacyjne prawidłowe wartości markerów nowotworowych nie wykluczają jednak choroby przerzutowej.
- AFP,
Biopsja6
- W
- Jeśli podejrzenie się potwierdzi, wykonuje się orchiektomię radykalną.
Wskazania do skierowania do specjalisty
PrzyWpodejrzeniuprzypadku podejrzenia nowotworu jądra, wątpliwego zapalenia najądrza lub zapalenia jądra, które nie ustępuje w- Jeśli wyniki badań są niejasne, należy niezwłocznie skierować pacjenta do urologa.
TerapiaLeczenie
Cele terapiileczenia
- Wyleczenie (u
- W
Ogólne informacje o terapii leczeniu
- Rozróżnienie między nasieniakami i
- Zasadniczo wskaźniki wyleczenia nowotworu jądra są bardzo wysokie. W
.
Leczenie chirurgiczne6
TerapiaLeczenie nowotworu jądra odbywa się zasadniczo przez orchiektomię.ChemoterapiChemioterapię można stosować jako leczenie pierwszej linii dopiero w
- W
- Operację oszczędzającą narzą
dydu można rozważyć w(<2 cm), zwłaszcza jeśli występuje obustronne zajęcie, jedno zajęte jądro lub zanik jądra przeciwległego.>. - Na życzenie pacjenta można wszczepić protezę jądra.
- Przy preparowaniu węzłów chłonnych zaotrzewnowych (retroperitoneal lymph node dissection — RPLND) usuwa się węzły chłonne znajdujące się w
terapiileczeniu nienasieniaków, zarówno wchemoterapiichemioterapii.
Farmakoterapia
ChemoterapiaChemioterapia6
- Najskuteczniejszymi cytostatykami w
- Standardowym leczeniem w
- W
- W
Radioterapia
Tę sekcjSekcję opracowano na podstawietychnastępujących źródeł:6,1819.- Nasieniaki są bardzo wrażliwe na promieniowanie; w
nasieniakowychbardzo skuteczne są zarówno radioterapia, jak ichemoterapiachemioterapia. - W
- Wykazano, że po orchiektomii 80–85% pacjentów nie wymaga dalszego leczenia.
1920. - Szanse na wyleczenie i
- Terapia radiacyjna może prowadzić do długotrwałych następstw, takich jak wtórne nowotwory złośliwe czy choroby układu krążenia.
- Radioterapia może przejściowo powodować złe samopoczucie, biegunkę i
TerapiaLeczenie nasieniaków4,6,1819
| Stopnia 1. |
|
| Stopnia 2. |
|
| Stopnia 3. |
|
Leczenie nienasieniaków
| Stopnia 1. |
|
| Stopnia 2. |
|
| Stopnia 3. |
|
Nawroty
- Leczenie nawrotu zależy od rokowania.
- korzystne rokowanie: odpowiedź całkowita na leczenie pierwszego rzutu, niskie stężenie biomarkerów nowotworowych w
- niekorzystne rokowanie: niepełna odpowiedź na leczenie pierwszego rzutu, wysokie stężenie biomarkerów nowotworowych w
- korzystne rokowanie: odpowiedź całkowita na leczenie pierwszego rzutu, niskie stężenie biomarkerów nowotworowych w
- Późny nawrót: nawrót występujący nie wcześniej niż po upływie 2 lat po terapii pierwszego rzutu
- Leczenie obejmuje ponowną resekcję, jeśli jest to technicznie możliwe.
- Alternatywnie w
chemoterapichemioterapię lubchemoterapichemioterapię wysokodawkową, a
Płodność6
- U
- Mężczyznom w
terapiileczenia poddali się analizie nasienia i
Leczenie paliatywne
- Jeśli choroba nie jest wyleczalna, należy na wczesnym etapie omówić z
Zalecenia dla pacjentów
- Bardzo ważna jest staranna realizacja programu badań kontrolnych.
- Jeśli pacjent wyraża chęć posiadania dzieci, przed rozpoczęciem
terapiileczenia należy rozważyć analizę i
Przebieg, powikłania i rokowanie
Przebieg
- Nawroty po leczeniu występują w
Powikłania
- W
2021. - U
2122-2223. - Jeśli pacjent chce mieć dzieci, należy mu zaproponować analizę i
. - Możliwe są zmniejszone libido, wytrysk wsteczny, zaburzenia erekcji i
2324. - Niedobór testosteronu6
WtRzadko wtórne nowotwory złośliwe (białaczki)— rzadko- Działania niepożądane
chemoterapiichemioterapii- utrata słuchu lub szumy uszne — w
>>300 toksycznośćuszkodzenie płucnauc inerkowanerek- Bardzo złe samopoczucie podczas przyjmowania cisplatyny. Wymagane jest kompleksowe leczenie przeciwwymiotne antagonistami 5-HT3 w
- Neurotoksyczności można zapobiec lub ją ograniczyć poprzez staranne nawodnienie podczas podawania cisplatyny.
ŚrodkiLekitoksyczne dla nereknefrotoksyczne, takie jak aminoglikozydy, są przeciwwskazane podczas leczenia cisplatyną.2425.
- utrata słuchu lub szumy uszne — w
Rokowanie
Tę sekcjSekcję opracowano na podstawietychnastępujących źródeł:4,6.- Rokowanie jest zasadniczo bardzo dobre.
- Niezależne od stopnia zaawansowania, wskaźnik 5-letnich przeżyć u
- U
- Nawet w
- Wskaźnik 5-letnich przeżyć w
- Wskaźnik 5-letnich przeżyć w
- Korzystne
rokowaniarokowanie zależy w - Im bardziej zaawansowana choroba, tym większe ryzyko nawrotu.
Prawdopodobieństwo przeżycia w przypadku guzów zarodkowych jądra
Dalsze postępowanie
- Zalecane są regularne kontrole
przebieguw - Celem jest wykrycie nawrotów lub przerzutów, a
- Większość nawrotów występuje w
- Badanie kontrolne obejmuje6
:- wywiad lekarski, badanie przedmiotowe, badanie palpacyjne węzłów chłonnych nad- i
- oznaczenie biomarkerów nowotworowych (AFP,
HCGhCG, LDH), poziomu lipidów icukruglukozy we krwi, poziomu hormonów, pomiar ciśnienia tętniczego, masy ciała, BMI - kontrola ultrasonograficzna drugiego jądra oraz ewentualnie szczątkowego miąższu jądra
- RTG klatki piersiowej
- TK jamy brzusznej i
- wywiad lekarski, badanie przedmiotowe, badanie palpacyjne węzłów chłonnych nad- i
Dalsze postępowanie w zależności od stopnia zaawansowania
- Schemat postępowania po leczeniu zależy od rodzaju nowotworu oraz stopnia zaawansowania, a
- W
procedurbadań obrazowych.- Schematy dalszego postępowania dostosowane do stopnia zaawansowania nowotworu nie wykazują przewagi pod względem wskaźników przeżycia nad standardowym schematem dalszego postępowania.
- Zmodyfikowane schematy dalszego postępowania są stosowane przede wszystkim w
Informacje dla pacjentów
Informacje dla pacjentów w Deximed
Informacje ogólne
- Terapie nowotworowe, leki
- Przygotowanie do terapii radiacyjnej
- Ból i
- Jeśli jesz bardzo mało — poradnik żywieniowy
Rak a seksualność
- Rak a
- Rak a
- Rak a
opiekaOpieka paliatywna w zaawansowanej chorobie nowotworowej
- Leki w
- Leczenie lęku
- Nudności i
- Zaparcia
- Suchość błony śluzowej jamy ustnej
- Trudności z
- Utrata masy ciała w
- Depresja
- Majaczenie
Ilustracje
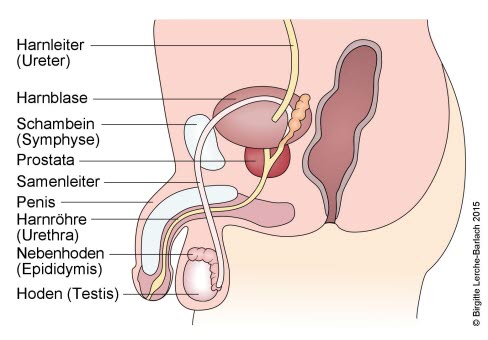
Męskie narządy płciowe
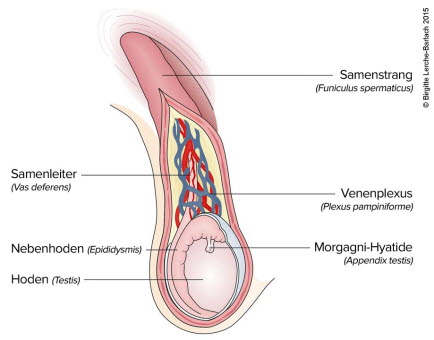
Prawidłowe jądro
QuellenŹródła
LeitlinienWytyczne
- Albers P, Algaba F, Bokemeyer C, et al. Guidelines on testicular cancer. European Association of Urology (EAU). Stand 2020.
- Oldenburg J, Fossa SD, Nuver J, et al. Testicular seminoma and non-seminoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology 2013;24 (suppl 6):vi125-vi132.
- Stelmach A, Potemski P. [Red]. Nowotwory układu moczowo-płciowego. Zalecenia postępowania diagnostyczno-terapeutycznego w nowotworach złośliwych — 2013 r. (dostęp 30.12.2023) onkologia.zalecenia.med.pl
LiteraturPiśmiennictwo
- Sobin LH, Witterkind C: TNM classification of malignant tumours., UICC Wiley-Liss, 2007.
- International Germ Cell Consensus Classification: a prognostic factor- based staging system for metastatic germ cell cancers. International Germ Cell Cancer Collaborative Group. J Clin Oncol 1997; 15: 594-603. PubMed
- Gangireddy Vgr, Liles GB, Sostre GD, Coleman T. Response of metastatic renal medullary carcinoma to carboplatinum and Paclitaxel chemotherapy. Clin Genitourin Cancer 2012; 10(2): 134-9. pmid:22409864
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=22409864[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=22409864[uid]" target="_blank">PubMed - Oldenburg J, Fossa SD, Nuver J, Heidenreich A, Schmoll HJ, Bokemeyer C, Horwich A, Beyer J, Kataja V. Testicular seminoma and non-seminoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology 2013;24(suppl 6):vi125-vi132.
http://www.esmo.org/Guidelines/Genitourinary-Cancers/Testicular-Seminoma-and-Non-Seminoma" href="http://www.esmo.org/Guidelines/Genitourinary-Cancers/Testicular-Seminoma-and-Non-Seminoma" target="_blank">www.esmo.org - Ye H, Ulbright TM. Difficult differential diagnoses in testicular pathology. Arch.Pathol.Lab.Med 2012; 136(4): 435-46. pmid:22458906
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=22458906[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=22458906[uid]" target="_blank">PubMed - Albers P, Algaba F, Bokemeyer C, et al. Guidelines on testicular cancer. European Association of Urology (EAU). Stand 2020.
http://uroweb.org/guideline/testicular-cancer/" href="http://uroweb.org/guideline/testicular-cancer/" target="_blank">uroweb.org - Chia VM, Quraishi SM, Devesa SS, Purdue MP, Cook MB, McGlynn KA. International trends in the incidence of testicular cancer, 1973-2002. Cancer Epidemiol Biomarkers Prev. 2010 May. 19(5):1151-9.
https://pubmed.ncbi.nlm.nih.gov/20447912/" href="https://pubmed.ncbi.nlm.nih.gov/20447912/" target="_blank">pubmed.ncbi.nlm.nih.gov - Horwich A, Shipley J, Huddart R. Testicular germ-cell cancer. Lancet 2006; 367: 754-65. PubMed
- Rabijewski M. Nowotwory jąder. (dostęp 29.12.2023) podyplomie.pl
- Bazzi WM, Raheem OA, Stroup SP, Kane CJ, Derweesh IH, Downs TM. Partial orchiectomy and testis intratubular germ cell neoplasia: World literature review. Urol.Ann 2011; 3(3): 115-8. pmid:21976922
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=21976922[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=21976922[uid]" target="_blank">PubMed - Wood HM, Elder JS. Cryptorchidism and Testicular Cancer: Separating Fact From Fiction. The Journal of Urology 2009; 181(12): 452-61. pmid:19084853
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=19084853[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=19084853[uid]" target="_blank">PubMed - Cook MB, Akre O, Forman D, Madigan MP, Richiardi L, McGlynn KA. A systematic review and meta-analysis of perinatal variables in relation to the risk of testicular cancer-experiences of the son. Int J Epidemiol 2010; 396: 1605-18. pmid:20660640
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=20660640[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=20660640[uid]" target="_blank">PubMed - Peng X, Zeng X, Peng S, Deng D, Zhang J. The association risk of male subfertility and testicular cancer: a systematic review. PloS one 2009; 4(5): e5591. pmid:19440348
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=19440348[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=19440348[uid]" target="_blank">PubMed - Neale RE, Carriere P, Murphy MFG, Baade PD. Testicular cancer in twins: A meta-analysis. British Journal of Cancer 2008; 98(1): 171-3. pmid:18071360
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=18071360[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=18071360[uid]" target="_blank">PubMed - Shephard EA, Hamilton WT. Selection of men for investigation of possible testicular cancer in primary care: a large case-control study using electronic patient records. Br J Gen Pract 2018. pmid:29970393
https://www.ncbi.nlm.nih.gov/pubmed?cmd=Search&term=29970393%5Buid%5D" href="https://www.ncbi.nlm.nih.gov/pubmed?cmd=Search&term=29970393%5Buid%5D" target="_blank">www.ncbi.nlm.nih.gov - Naveed S, Quari H, Sharma H. Cavernous haemangioma of the testis mimicking as testicular malignancy in an adolescent. Scott.Med.J 2013; 58(4): e5-e7. pmid:24215057
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=24215057[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=24215057[uid]" target="_blank">PubMed - Lokesh KN, Sathyanarayanan V, Lakshmaiah KC, Suresh TM, Dasappa L, Kanakasetty GBK. Primary Diffuse large B-Cell lymphoma of testis: A single centre experience and review of literature. Urol.Ann 2014; 6(3): 231-4. pmid:25125896
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=25125896[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=25125896[uid]" target="_blank">PubMed - Venkitaraman R, Johnson B, Huddart RA et al. The utility of lactate dehydrogenase in the follow-up of testicular germ cell tumours. BJU Int 2007; 100: 30-2. PubMed
- Alberta Health Services (AHS). Testicular germ cell tumours. Clinical Practice Guideline GU-001, version 7. Edmonton: AHS; 2016.
http://www.albertahealthservices.ca/assets/info/hp/cancer/if-hp-cancer-guide-gu001-testicular.pdf" href="http://www.albertahealthservices.ca/assets/info/hp/cancer/if-hp-cancer-guide-gu001-testicular.pdf" target="_blank">www.albertahealthservices.ca - Choo R, Thomas G, Woo T et al. Long-term outcome of postorchiectomy surveillance for stage I testicular seminoma. Int J Radiat Oncol Biol Phys 2005; 61: 736-40. PubMed
- Abouassaly R, Fossa SD, Giwercman A, Kollmannsberger C, Motzer RJ, Schmoll HJ, Sternberg CN. Sequelae of treatment in long-term survivors of testis cancer. Eur.Urol 2011; 60(3): 516-26. pmid:21684072
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=21684072[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=21684072[uid]" target="_blank">PubMed - Cvancarova M, Samuelsen SO, Magelssen H, Fossa SD. Reproduction rates after cancer treatment: experience from the Norwegian radium hospital. J Clin Oncol 2009; 27(3): 334-43. pmid:19075285
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=19075285[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=19075285[uid]" target="_blank">PubMed - Molnar Z, Mokanszki A, Bazsane ZK, Bhattoa HP, Benyo M, Olah E, Jakab A. Sperm concentration, hyaluronic acid-binding capacity, aneuploidy and persistent histones in testicular cancer. Hum.Reprod 2014; 29(9): 1866-74. pmid:25047166
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=25047166[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=25047166[uid]" target="_blank">PubMed - Carpentier MY, Fortenberry JD. Romantic and sexual relationships, body image, and fertility in adolescent and young adult testicular cancer survivors: A review of the literature. J.Adolesc.Health 2010; 47(2): 115-25. pmid:20638003
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=20638003[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=20638003[uid]" target="_blank">PubMed - Souchon R, Hartmann M, Krege S, Lorch A, Mayer F, De Santis M, Gillessen S, Beyer J, Cathomas R. Interdisciplinary Evidence-Based Recommendations for the Follow-Up of Early Stage Seminomatous Testicular Germ Cell Cancer Patients. Strahlenther Onkol 2011; (3): 158-66. pmid:21347634
http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=21347634[uid]" href="http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=PubMed&term=21347634[uid]" target="_blank">PubMed
Autor*innenAutorzy
- Michał Sutkowski, lekarz, specjalista medycyny rodzinnej, NZOZ Medycyna Rodzinna w Osuchowie (recenzent)
- Tomasz Tomasik, Dr hab. n. med., Prof. UJ, specjalista medycyny rodzinnej, Uniwersytet Jagielloński Collegium Medicum w Krakowie (redaktor)
- Laura Morshäuser,
Ärztinlekarz, Freiburg im Breisgau - Jessica Lobitz, B. Sc., Deutsche Krebsgesellschaft, Berlin