Informacje ogólne
Definicja
- Astma jest przewlekłą chorobą zapalną dróg oddechowych, która prowadzi do wystąpienia objawów oddechowych na skutek nadreaktywności oskrzeli i odwracalnej obturacji dróg oddechowych.
- Typowe objawy to napadowy kaszel, duszność i uczucie ucisku w klatce piersiowej.
- Podstawowe rozróżnienie obejmuje następujące postaci:
- astma alergiczna (zewnątrzpochodna)
- Czynnikami wyzwalającymi są specyficzne alergeny.
- związek z innymi chorobami alergicznymi/atopowymi
- astma niealergiczna (wewnątrzpochodna)
- Czynnikami wyzwalającymi są np. zakażenia dróg oddechowych lub nietolerancja leków (często ASA lub NLPZ).
- Inne fenotypy
- np. astma eozynofilowa lub kaszlowy wariant astmy (cough variant asthma — CVA)
- astma alergiczna (zewnątrzpochodna)
Definicja ciężkiej astmy
- U dzieci i młodzieży ciężka astma występuje, jeśli przy odpowiednim i adekwatnym leczeniu, mającym na celu dobrą kontrolę astmy, konieczne jest stałe (>6 miesięcy) stosowanie dodatkowego leczenia długo działającym lekiem antycholinergicznym (LAMA) lub przeciwciałem monoklonalnym i/lub podawanie dużej dawki dziennej glikokortykosteroidów wziewnych (wGKS).
Częstość występowania
- Na astmę choruje około 10% dzieci w Europie.
- Astma jest najczęstszą chorobą przewlekłą wieku dziecięcego1.
- W przeciwieństwie do dorosłych, chłopcy chorują częściej niż dziewczęta.
- U dzieci jest to głównie astma alergiczna.
- Podczas gdy współczynnik chorobowości astmy w świecie zachodnim wzrósł w ostatnich dekadach, liczba hospitalizacji i zgonów znacznie się zmniejszyła.
- W skali świata w 2015 roku około 358 milionów osób chorowało na astmę oskrzelową, a liczbę zgonów z powodu tej choroby szacowano na 400 0002.
- Jako możliwe przyczyny wzrostu częstości występowania w ostatnich dekadach rozważa się:
- Wydaje się, że rosnący od dawna współczynnik chorobowości astmy osiągnął ostatnio w świecie zachodnim ustabilizowany poziom8.
Etiologia i patogeneza
- Astma to choroba heterogeniczna o różnych mechanizmach patofizjologicznych.
- Rozwój astmy jest wieloczynnikowy, obejmuje uwarunkowania genetyczne i czynniki egzogenne, a także jest wzmocniony przez aspekty psychospołeczne.
- Warunki życia, takie jak odżywanie i higiena, prawdopodobnie odgrywają znaczącą rolę, ponieważ istnieją duże różnice w częstości występowania astmy między różnymi regionami świata.
Przyczyny astmy
- Czynniki genetyczne i epigenetyczne
- Czynniki środowiskowe
- Zanieczyszczenie powietrza, np. spowodowane ruchem drogowym w miastach, wydaje się być związane z wyższym ryzykiem wystąpienia astmy7.
- Zanieczyszczenie i alergeny w pomieszczeniach, np. roztocza kurzu domowego, dym lub sierść zwierząt mogą przyczynić się do rozwoju astmy9.
- Narażenie na dym papierosowy w czasie ciąży i we wczesnym dzieciństwie prowadzi do zwiększonego ryzyka zachorowania.
- W Szkocji po wprowadzeniu zakazu palenia w 2006 roku zaobserwowano roczny spadek liczby hospitalizacji dzieci z astmą o 18%10.
- Dzieciństwo spędzone na wsi w gospodarstwie rolnym (różnorodność mikroorganizmów) ma działanie ochronne6,11.
- Ekspozycja na zwierzęta
- Nawracające wirusowe zakażenia górnych dróg oddechowych we wczesnej fazie życia
- Nie jest jasne, czy zakażenia biorą udział w rozwoju astmy, czy też jej zapobiegają (hipoteza higieniczna).
- W jednym z badań stwierdzono, że zmniejszają one ryzyko rozwoju astmy do wieku szkolnego13.
- Jednak wydaje się, że zakażenia wirusowe układu oddechowego, zwłaszcza zakażenia RSV i wywołane przez rinowirusy są istotne zarówno dla występowania astmy, jak i wywoływania ostrych napadów astmatycznych.
- Uważa się, że około 80–95% zaostrzeń astmy u dzieci w wieku szkolnym jest związanych z wirusowymi zakażeniami dróg oddechowych14.
- Otyłość
- Związek z zaburzeniami atopowymi16-19
- Leki
- Metaanaliza dowodzi, że przyjmowanie paracetamolu we wczesnym okresie życia jest związane z późniejszym rozwojem astmy20.
- W prospektywnym badaniu kohorty urodzeniowej 620 dzieci z historią alergii w rodzinie nie stwierdzono związku między przyjmowaniem paracetamolu a rozwojem astmy21.
- Leczenie antybiotykami o szerokim spektrum działania w okresie rozwoju płodowego i we wczesnym okresie życia może być związane ze zwiększoną częstością występowania astmy. Wciąż jednak brakuje jednoznacznego potwierdzenia22-23.
- Zaleca się, aby paracetamol i antybiotyki o szerokim spektrum działania były stosowane w ciąży i pierwszej fazie życia dziecka tylko w przypadku wyraźnych wskazań.
Patogeneza
- Proces chorobowy w przypadku astmy jest bardzo zróżnicowany.
- Podział postaci astmy na fenotypy wynika z założenia, że choroba u niektórych grup pacjentów charakteryzuje się zarówno podobną patofizjologią, jak i podobnymi cechami klinicznymi.
- Wyróżnia się następujące fenotypy:
- Astma alergiczna (zewnątrzpochodna)
- skłonność do atopii
- często z towarzyszącą alergią
- wykrywanie specyficznych IgE w surowicy
- przebieg sezonowy (np. pyłki traw) lub wieloletni (np. roztocza kurzu domowego)
- astma niealergiczna (wewnątrzpochodna)
- bez potwierdzenia uczulenia
- czynnik wyzwalający to często zakażenie dróg oddechowych
- inne szczególne postacie (patrz następna sekcja)
- Astma alergiczna (zewnątrzpochodna)
- Astma może wpływać na drogi oddechowe na różne sposoby:
- zmiany w błonach śluzowych
- zmiany w odpowiedzi immunologicznej
- zmiany w odpowiedzi nerwowo-mięśniowej
- zmiany w zaopatrzeniu naczyniowym
- W drogach oddechowych występuje zwykle zwiększona ilość granulocytów kwasochłonnych, komórek tucznych, limfocytów T oraz mediatorów zapalnych i innych cytokin.
- Czynniki zapalne i wzrostowe prowadzą do przerostu i hiperplazji mięśni gładkich, co skutkuje niedrożnością.
- Zmieniona jest aktywność odruchowa i wrażliwość ściany oskrzeli, co przyczynia się do nadreaktywności oskrzeli.
Szczególne postacie astmy
- Astma „typu 2” lub astma typu „2 high”
- W oparciu o stwierdzenie, że pewne cytokiny, takie jak IL-5 i IL-13, mogą być uwalniane nie tylko przez swoiste dla alergenu limfocyty T pomocnicze, ale także przez nieswoiste dla alergenu naturalne komórki limfoidalne (ILC2 (innate lymphoid cells — ILC2)).
- Powiązane markery stanu zapalnego — eozynofile we krwi i wydychany tlenek azotu — nazywane są „biomarkerami typu 2”.
- Z jednej strony, zapalenie typu 2 zwykle dobrze reaguje terapeutycznie na wziewne glikokortykosteroidy (wGKS) i doustne glikokortykosteroidy (dGKS); z drugiej strony, wGKS i dGKS znacząco wpływają na markery zapalenia typu 2.
- Kontrowersyjne jest, czy fenotyp typu „2 low” w ogóle istnieje w klasycznej astmie. W przypadku wykrycia niskich markerów typu 2 należy sprawdzić, czy
- Może istnieć inne rozpoznanie, które przypomina astmę.
- Przewlekłe zakażenie nakłada się na proces zapalny.
- Markery typu 2 są jatrogennie tłumione przez leczenie wysokimi dawkami glikokortykosteroidów.
- Proponuje się następujące wartości progowe dla zapalenia typu 2 dla pacjentów z astmą, leczonych obecnie GKS:
- granulocyty kwasochłonne we krwi ≥150/mikrolitr — i/lub —
- tlenek azotu w wydychanym powietrzu (FeNO) ≥20 ppb — i/lub —
- granulocyty kwasochłonne w plwocinie ≥2% — i/lub —
- patogeneza alergiczna (dodatni wywiad lekarski w połączeniu z potwierdzeniem odpowiedniego uczulenia na typowe alergeny obecne w powietrzu)
- Astma eozynofilowa a nieeozynofilowa
- Rozróżnienie podtypów odbywa się głównie na podstawie badania plwociny oraz morfologii krwi z rozmazem.
- Wartość progowa stężenia eozynofilów we krwi, powyżej której można mówić o eozynofilii, nie została jeszcze jednoznacznie wyjaśniona.
- Gdyby postulować wartość progową 150 eozynofili/mikrolitr, większość byłaby „eozynofilowa”. Gdyby postulować wartość progową 300 eozynofili/mikrolitr, większość byłaby „nieeozynofilowa”.
- przydatna definicja: dwukrotne wykrycie ≥300 eozynofili/mikrolitr krwi poza zaostrzeniami w ciągu ostatnich 2 lat
- Ważne z terapeutycznego punktu widzenia jest to, że pacjenci z astmą eozynofilową i nieeozynofilową różnią się znacząco pod względem odpowiedzi na GKS.
- Co więcej, klasyfikacja ta staje się coraz ważniejsza dla wskazań do terapii biologicznej, ponieważ wzrost liczby eozynofili zwiększa prawdopodobieństwo odpowiedzi na niektóre leki biologiczne (omalizumab, dupilumab, tezepelumab) lub w ogóle jest warunkiem odpowiedzi (leki biologiczne anty-IL-5).
- „Kaszlowy wariant astmy”
- Pacjenci cierpią na przewlekły, suchy kaszel spowodowany nieswoistą nadreaktywnością oskrzeli bez innych typowych objawów astmy (duszności, świstów, furczenia).
- Czynność płuc i zdjęcie RTG narządów klatki piersiowej są w normie.
- U 1/3 pacjentów z kaszlowym wariantem astmy dochodzi do rozwoju astmy klasycznej.
- Pacjenci z kaszlowym wariantem astmy dobrze reagują na klasyczne opcje leczenia przeciwastmatycznego, a wczesne leczenie może zapobiec rozwinięciu się astmy klasycznej.
- Choroba układu oddechowego nasilana przez aspirynę (Aspirin Exacerbated Respiratory Disease — AERD)
- wcześniej znana jako: „astma z nietolerancją aspiryny”
- nietolerancja inhibitorów cyklooksygenazy-1 (COX-1), takich jak kwas acetylosalicylowy (ASA) lub ibuprofen
- Przyjmuje się, że ta nietolerancja farmakologiczna jedynie pogłębia istniejące wcześniej uszkodzenie układu oddechowego, ale go nie wywołuje.
- Dokładny współczynnik chorobowości jest niejasny i wynosi od 5% do 12% chorych na astmę.
- klasycznie towarzyszące polipy nosa i przewlekłe zapalenie zatok (zespół Samtera)
- Skurcz oskrzeli indukowany wysiłkiem fizycznym
- wcześniej znany jako: „astma wysiłkowa”
- Wysiłek fizyczny prowadzi do obturacji dróg oddechowych.
- Uważa się, że przyczyną jest powtarzające się wysuszanie błon śluzowych, które sprzyja przebudowie dróg oddechowych i rozwojowi nadreaktywności oskrzeli.
- Występuje często podczas uprawiania sportów wytrzymałościowych (zwiększony wysiłek oddechowy).
- Uwaga dla sportowców: leczenie beta-2-sympatykomimetykami (SABA) podlega przepisom Światowej Agencji Antydopingowej (World Anti-Doping Agency — WADA)!
Czynniki predysponujące
Czynniki, które mogą wpływać na rozwój lub przebieg astmy
- Predyspozycje genetyczne
- Dzieci z predyspozycjami genetycznymi (tzw. dzieci z grupy ryzyka) określane są w ten sposób na podstawie informacji, że przynajmniej jedno z rodziców lub rodzeństwa cierpi na zaburzenie atopowe.
- Obecność innych zaburzeń atopowych (np. wyprysk, nieżyt nosa)
- Dym tytoniowy
- Przyjmowanie antybiotyków i paracetamolu w czasie ciąży przez matkę23-24
- Stres psychospołeczny
- Otyłość15
Czynniki wyzwalające
- Zobacz również artykuł Napad astmatyczny u dzieci i młodzieży.
- Istnieje wiele czynników, które mogą wywołać ostry napad astmatyczny:
ICD-10
- J45 Astma oskrzelowa
- J45.0 Astma oskrzelowa w głównej mierze z przyczyn alergicznych
- J45.1 Astma oskrzelowa niealergiczna
- J45.8 Astma oskrzelowa mieszana
- J45.9 Astma oskrzelowa, nieokreślona
- J46 Stan astmatyczny, w tym ostra astma o ciężkim przebiegu
Diagnostyka
Kryteria diagnostyczne
- Rozpoznanie astmy powinno być ustalone na podstawie wywiadu lekarskiego, charakterystycznych objawów i wyników badań czynnościowych płuc oraz powinno uwzględniać typowe biomarkery.
- U małych dzieci, które nie są jeszcze w stanie współpracować przy badaniu czynności płuc, rozpoznanie jest trudniejsze. Oprócz rodzinnych i osobistych wskazań anamnestycznych dotyczących zaburzeń atopowych, należy zadać konkretne pytania/przeprowadzić badania:
- ≥3 epizody typowe dla astmy w ciągu ostatniego roku
- hospitalizacja z powodu objawów obturacji dróg oddechowych
- świszczące szmery oddechowe/suchy kaszel bez zakażenia, szczególnie podczas wysiłku fizycznego
- odpowiedź objawów na próbę leczenia lekami przeciwastmatycznymi
- wykrycie uczulenia na aeroalergeny i/lub eozynofilia we krwi
- Dodatni wynik próby rozkurczowej, w połączeniu z typowymi objawami astmy, potwierdza rozpoznanie astmy.
- Nawet w przypadku braku rozkurczu przy SABA, astmę można rozpoznać, jeśli istnieją inne oznaki astmy (podwyższone markery typu 2 i odpowiedź na leczenie GKS).
Ostry napad astmatyczny
- Informacje na temat diagnostyki i leczenia ostrego napadu astmatycznego można znaleźć w artykule Napad astmatyczny u dzieci i młodzieży.
Diagnostyka różnicowa
Niemowlęta
- Obturacyjne zapalenie oskrzeli wywołane przez wirusy
- Zapalenie oskrzelików (RSV)
- Wrodzona wada serca
- Aspiracja ciała obcego
- Mukowiscydoza
- Wrodzone anomalie, np. rozmiękanie tchawicy i oskrzeli
Małe dzieci
- Zapalenie oskrzelików
- Podgłośniowe zapalenie krtani
- Zapalenie nagłośni
- Krztusiec
- Aspiracja ciała obcego
- Wirusowe zapalenie oskrzeli
- Zapalenie płuc
- Mukowiscydoza
- Cukrzycowa kwasica ketonowa
- Refluks żołądkowo-przełykowy (objawy głównie w nocy i podczas leżenia)
Dzieci i młodzież
- Przewlekłe zapalenie oskrzeli
- Zapalenie płuc
- Odma opłucnowa
- Hiperwentylacja
- Cukrzycowa kwasica ketonowa
- Aspiracja ciała obcego
- Psychogenne problemy z oddychaniem
- Dysfunkcja strun głosowych (Vocal Cord Dysfunction — VCD)
- Refluks żołądkowo-przełykowy (objawy głównie w nocy i podczas leżenia)
Wywiad lekarski
Typowe dolegliwości
- Napadowa duszność, często w nocy
- Suchy kaszel bez zakażenia, podczas wysiłku fizycznego lub po nim
- Dodatkowe szmery wydechowe (świsty, furczenie, gwizdanie)
- Uporczywy nocny kaszel bez zakażenia
Wywiad dotyczący astmy
- Czynniki wyzwalające
- np. bodźce oddechowe, pora dnia i roku, miejsce i aktywność
- u dzieci często wysiłek fizyczny (sport, zabawa, także śmiech)
- narażenie na alergeny (np. zwierzęta domowe i pleśń)
- Czynniki ryzyka
- np. atopia (wyprysk, nieżyt nosa) w wywiadzie osobistym lub rodzinnym
- Choroby współwystępujące
- np. choroby górnych dróg oddechowych, otyłość, refluks żołądkowo-przełykowy
Cechy szczególne okresu dzieciństwa i dojrzewania
- Pytanie dotyczące biernego narażenia na dym tytoniowy
- W przypadku nastolatków pytanie o czynne palenie i aspiracje zawodowe
- możliwość podjęcia działań zapobiegawczych
- Wywiad lekarski jest szczególnie ważny u dzieci w wieku ≤5 lat (brak zdolności do współpracy w zakresie badania czynności płuc).
- U większości dzieci objawy astmy pojawiają się przed ukończeniem 5. roku życia25.
- W przypadku małych dzieci w wywiadzie lekarskim należy zwrócić uwagę na następujące kwestie:
- Nawracające epizody kaszlu przypominającego krztusiec mogą wskazywać na astmę26.
- Niektóre dzieci nie potrafią jasno opisać swoich objawów lub uciekają się do innych określeń.
Badanie przedmiotowe
- Ma na celu wykrycie oznak obturacji dróg oddechowych.
- Wyniki badań mogą nie budzić zastrzeżeń w odstępie czasowym.
- Możliwe wyniki badania
- stridor wydechowy
- wydłużony wydech
- suche szmery dodatkowe (świsty, gwizdy, furczenia) podczas osłuchiwania, w razie potrzeby prowokowane poprzez wymuszony wydech
- hipersoniczny dźwięk przy opukiwaniu, spowodowany rozdęciem płuc w ciężkiej astmie
- w przypadku ciężkiej niedrożności: bardzo cichy szmer oddechowy
- U dzieci należy zwrócić dodatkową uwagę na:
- oznaki atopii, np. wyprysk atopowy
- retrakcje szyjne, międzyżebrowe i nadbrzuszne jako oznaki duszności
- zwiększenie średnicy klatki piersiowej w wyniku hiperinflacji
- oznaki niedowagi i dystrofii u dziecka (zwiększony wysiłek oddechowy)
- wykluczenierozpoznań różnicowych (np. mukowiscydozy, niedoboru odporności, dysfunkcji rzęsek itp.)
Badania uzupełniające w praktyce lekarza rodzinnego
- Możliwość wykonania badań diagnostycznych u dzieci zależy od ich wieku i zdolności do współpracy.
- Wiarygodna diagnostyka czynności płuc jest często możliwa dopiero po 4.–5. roku życia.
Diagnostyka czynności płuc
- Aby potwierdzić rozpoznanie astmy, należy wykazać zmienną, (częściowo) odwracalną obturację dróg oddechowych za pomocą badania czynnościowego płuc, zwykle spirometrii.
- Prawidłowe wyniki badań czynnościowych płuc nie wykluczają astmy.
Spirometria z uwidocznieniem pełnej krzywej przepływ-objętość
- Pomiar nasilonej pojemności życiowej (forced vital capacity — FVC), nasilonej jednosekundowej objętości wydechowej (forced expiratory volume in one second — FEV1) i stosunku FEV1/FVC (wskaźnik Tiffeneau)
- W celu kontroli jakości należy zarejestrować co najmniej trzy akceptowalne próby. Różnica między największą i drugą co do wielkości wartością FEV1 i FVC nie powinna być większa niż 5% i mniejsza niż 150 ml.
- Obraz obturacyjnych zaburzeń wentylacji
- zmniejszenie zależnego od wieku ilorazu FEV1 i FVC (wskaźnik Tiffeneau)
- zmniejszenie bezwzględnej pojemności jednosekundowej
- zmniejszenie szczytowego przepływu wydechowy (PEF peak expiratory flow)
- Ocena w odniesieniu do wartości referencyjnych dla danego wieku w ramach wytycznych Global Lung Initiative
- Specyfika u dzieci ≤5 lat
- Spirometrię można przeprowadzić tylko wtedy, gdy dzieci odpowiednio współpracują.
- Stosunek wielkości dróg oddechowych do objętości płuc u młodszych dzieci sprawia, że konieczne jest udokumentowanie dodatkowych parametrów czynności płuc (FEV0,5 i FEV0,75).
- Nawet jeśli czas wydechu jest dłuższy niż 1 s, stosunek FEV1/FVC wynosi 0,9 u zdrowych dzieci w wieku do 6 lat.
- W związku z tym wartości te nie mogą być wykorzystywane do oceny niedrożności dróg oddechowych u dzieci przed osiągnięciem wieku szkolnego, co jest możliwe u starszych dzieci.
- Często ocena obturacyjnego zaburzenia wentylacji jest możliwa dopiero po wykonaniu próby rozkurczowej.
Próba rozkurczowa
- U pacjentów z potwierdzoną obturacją dróg oddechowych należy najpierw wykonać próbę rozkurczową z krótko działającymi SABA w celu potwierdzenia rozpoznania.
- Spirometria przed i 15 minut po podaniu wziewnym SABA
- u dzieci podanie wziewne do 4 dawek SABA z inhalatora ciśnieniowego dozującego (np. salbutamol po 100 mcg)
- alternatywnie ponowna spirometria po 6–8 tygodniach leczenia wGKS w celu oceny rozkurczu
- Wzrost FEV1 >12% jest uznawany za dodatni.
- Kryterium bezwzględnego wzrostu o 200 ml, wymagane w przypadku osób dorosłych, zwykle nie ma zastosowania ze względu na mniejsze objętości.
- Zawsze należy oceniać kształt krzywej przepływ-objętość: nawet przy liczbowo niewystarczającym wzroście FEV1 normalizacja pierwotnie wklęsłego zdeformowanego ramienia wydechowego może wskazywać na astmę wymagającą leczenia.
- Cechy szczególne wieku dziecięcego (≤5 lat)
- w przypadku niedrożności osłuchowej sprawdzenie rozkurczu po podaniu SABA
Pomiar nadreaktywności (test prowokacyjny)
- Pomiar nadreaktywności dróg oddechowych jest zasadny w przypadku odpowiedniego podejrzenia, pod warunkiem, że wywiad lekarski wskazuje na astmę, ale nie ma objawów klinicznych i/lub potwierdzenia obturacyjnego zaburzenia wentylacji.
- Wymagania: przestrzeganie przeciwwskazań i doświadczenie użytkowników
- Metody wykonania próby prowokacyjnej
- nieswoiste wziewne wywołanie z użyciem środków farmaceutycznych (np. metacholiny)
- standaryzowane obciążenie (za pomocą bieżni lub, szczególnie w przypadku małych dzieci, „testu swobodnego biegu”)
- prowokacja zimnym powietrzem
- U dzieci z objawami podczas wysiłku fizycznego zaleca się wykonanie próby wysiłkowej w biegu.
- Próbę uznaje się za dodatnią w następujących przypadkach:
- spadek FEV1 o ≥20% lub podwojenie swoistego oporu dróg oddechowych przy prowokacji farmakologicznej
- spadek FEV1 o ≥10% u dorosłych i ≥12% u dzieci i młodzieży podczas wysiłku fizycznego
Pletyzmografia całego ciała
- Umożliwia określenie swoistego oporu dróg oddechowych i objętości gazu wewnątrz klatki piersiowej oraz nadaje się do obiektywizacji rozdęcia płuc.
- Ponadto możliwa jest jakościowa ocena wdechowego i wydechowego oporu dróg oddechowych.
- Pomocna również w przypadku słabej współpracy podczas badań spirometrycznych.
- Podczas gdy dobrze prowadzone dzieci w wieku przedszkolnym często są w stanie wykonać spirometrię, ze względu na umiejętność współpracy pełną pletyzmografię ciała można zwykle wykonać dopiero w wieku szkolnym.
Pomiar szczytowego przepływu wydechowego (peak expiratory flow — PEF)
- Brak znaczenia w diagnostyce podstawowej
- Astmy nie powinno się rozpoznawać wyłącznie na podstawie pomiaru szczytowego przepływu wydechowego (PEF).
- Jednak domowy pomiar wartości PEF jest przydatny do oceny przebiegu choroby i oceny kontroli astmy.
- Pomiar ma co najwyżej uzupełniające znaczenie.
- Pomiar dwa razy dziennie (rano i wieczorem, przed wziewnym podaniem leków) pozwala ocenić zmienność PEF.
- Regularne domowe pomiary przepływu szczytowego są stosowane w dzieciństwie głównie jako część edukacji pacjenta, zwłaszcza jeśli dziecko ma trudności z subiektywnym postrzeganiem objawów oddechowych.
- Nie ma jednak ogólnego zalecenia dla dzieci.
Badanie rentgenowskie
- Ogólnie niezalecane u dzieci i młodzieży
- w razie potrzeby zastosowanie do wykluczenia rozpoznań różnicowych w przypadku nietypowych objawów lub rozbieżnych wyników badań
- w tym przypadku jednak tylko zdjęcie tylno-przednie; dodatkowe zdjęcie boczne u dzieci i młodzieży uważa się za przestarzałe
Badania laboratoryjne
- Badania laboratoryjne nie są wymagane do rozpoznania, ale są przydatne w diagnostyce różnicowej.
- Przy braku odpowiedzi na leczenie, częstych zakażeniach oskrzeli, naciekach płucnych lub w ciężkiej astmie należy przeprowadzić uzupełniającą badania laboratoryjne dla celów diagnostyki różnicowej.
- liczba leukocytów oraz CRP w przypadku podejrzenia zaostrzenia zakażenia
- Bezwzględna liczba eozynofili (eozynofile/mikrolitr)
- im wyższa liczba eozynofili we krwi (i poziom FeNO), tym wyższe ryzyko zaostrzenia u pacjentów z astmą
- ważny marker prognostyczny odpowiedzi na leczenie lekami biologicznymi anty-IL-5 (R): im wyższa liczba eozynofili we krwi, tym bardziej prawdopodobna odpowiedź
- Całkowite IgE we krwi
- Wartości powyżej 100 kU/l wskazują na alergiczną przyczynę astmy.
- Wartości >1000 kU/l i powikłany przebieg wskazują na inną przyczynę problemów, np. zespół Churga-Strauss lub alergiczną aspergilozę oskrzelowo-płucną.
Diagnostyka specjalistyczna
Stężenie tlenku azotu (FeNO) w powietrzu wydychanym
- Nieinwazyjny biomarker stanu zapalnego dróg oddechowych
- Pomiar FeNO w dzieciństwie, okresie dojrzewania i dorosłości jest technicznie szybki i łatwy do wykonania (jeśli dostępne jest odpowiednie urządzenie) oraz możliwy do powtórzenia.
- Podwyższone poziomy FeNO w wydychanym powietrzu korelują z zapaleniem dróg oddechowych typu 2 u pacjentów z objawami astmy.
- Według American Thoracic Society dolne limity wynoszą 20 ppb (części na miliard) dla dzieci i 25 ppb dla dorosłych.
- Pacjenci z podwyższonym poziomem FeNO zazwyczaj reagują na GKS. I odwrotnie, zwiększone wartości FeNO (zwłaszcza wartości FeNO >50 ppb) podczas leczenia GKS przemawiają przeciwko zmniejszeniu dawki GKS pomimo stabilności klinicznej.
Alergologiczna diagnostyka stopniowa
- Patrz również artykuł Diagnostyka alergii u dzieci.
- U pacjentów z podejrzeniem astmy alergicznej
- Diagnostyka stopniowa
- wywiad dotyczący alergii, w tym wywiad zawodowy (w razie potrzeby kwestionariusz)
- alergiczne testy skórne (np. test punktowy)
- oznaczanie swoistych i całkowitych IgE
- test prowokacyjny
- diagnostyczne wyeliminowanie narażenia
Weryfikacja rozpoznania
- Rozpoznanie astmy należy zweryfikować lub zakwestionować:
- w przypadku niewystarczającej kontroli pomimo terapii zgodnej z wytycznymi - lub -
- po kilkumiesięcznej próbie uzyskania remisji, z uwzględnieniem sezonowych czynników wyzwalających
- Celem jest uniknięcie błędnego rozpoznania oraz nadmiernego lub niewłaściwego leczenia.
- Astmę nie zawsze udaje się rozpoznać już podczas wstępnego badania. Dlatego zasadne są obserwacje przebiegu, które dostarczają informacji o spontanicznych i/lub wywołanych lekami wahaniach obrazu klinicznego.
- GINA zaleca, aby rozważyć badanie niewydolności kory nadnerczy, gdy pacjenci są trwale uzależnieni od dGKS lub wysokich dawek GKS + LABA26.
Wskazania do skierowania do specjalisty/hospitalizacji
- Wskazania do skierowania do pulmonologa (dziecięcego)
- Należy sprawdzić wskazanie skierowania:
- wątpliwości dotyczące rozpoznania
- niewystarczająca kontrola astmy pomimo intensywnego leczenia
- wcześniejsze leczenie w nagłych wypadkach
- Podejrzenie współistniejących chorób, które negatywnie wpływają na kontrolę astmy.
- Wskazane skierowanie:
- Dzieci i młodzież, u których astma wymaga leczenia na 4 lub 5 stopniu intensywności leczenia.
- wskazania i rozpoczynanie leczenia przeciwciałami monoklonalnymi u dzieci i młodzieży
- Przed przejściem do stopnia 5. lub 6. należy przeprowadzić rozszerzoną diagnostykę w ośrodku pneumologii dziecięcej.
- Należy sprawdzić wskazanie skierowania:
- Wskazania do hospitalizacji
- W przypadku ciężkiego lub zagrażającego życiu napadu astmatycznego po wstępnym leczeniu należy zorganizować natychmiastową hospitalizację, w razie potrzeby pod opieką lekarza pogotowia (w przypadku napadu zagrażającego życiu).
- Jeśli nie ma trwałej poprawy po 30–60 minutach od wstępnego postępowania w przypadku łagodnego lub umiarkowanego napadu astmatycznego, w ramach grupy wytycznych zaleca się natychmiastową hospitalizację lub dalsze leczenie na oddziale ratunkowym.
Leczenie
Cele leczenia
- Osiągnięcie i utrzymanie remisji astmy
- Unikanie:
- ostrych i przewlekłych przejawów choroby (np. objawów napadu astmatycznego)
- zaburzeń rozwoju fizycznego, psychicznego i umysłowego
- upośledzenia czynności życia codziennego (np. uprawiania sportu, aktywności społecznej)
- powikłań i szkód następczych
- niepożądanych skutków leczenia
- Poprawa jakości życia związanej ze zdrowiem i astmą
Ogólne informacje o leczeniu
Zasady leczenia astmy
- Aktualna koncepcja farmakologicznego leczenia astmy: odejście od zwalczania objawów za pomocą krótko działających leków o wielu reakcjach niepożądanych na rzecz zapobiegania objawom za pomocą trwale działających leków o niewielu reakcjach niepożądanych
- Podstawą leczenia jest stopień kontroli astmy.
- Zdefiniowano trzy stopnie kontroli astmy:
- astma kontrolowana
- astma częściowo kontrolowana
- astma niekontrolowana
- Obserwacja przebiegu choroby i powtórna ocena kontroli astmy
- ocena celów terapii i w razie potrzeby adaptacja (intensyfikacja/redukcja)
- Zdefiniowano trzy stopnie kontroli astmy:
- Unikanie czynników wyzwalających (np. narażenia na alergeny)
- Długotrwała i stopniowa farmakoterapia
- minimalizacja zużycia leków doraźnych poprzez długotrwałą terapię przeciwzapalną
- Informacje i edukacja pacjentów dla osób dotkniętych chorobą i ich krewnych
- W przypadku astmy alergicznej ewentualnie próba wczesnego odczulania
- Informacje na temat leczenia osób dorosłych można znaleźć również w artykule Astma.
- Aby uzyskać informacje na temat leczenia stanu ostrego w przypadku napadu astmatycznego, zobacz też:
Ocena przebiegu: stopień kontroli astmy
- Podział na trzy stopnie w zależności od dolegliwości, ograniczeń w życiu codziennym i stosowania leków doraźnych:
- astma kontrolowana
- astma częściowo kontrolowana
- astma niekontrolowana
- Patrz tabela Stopnie kontroli astmy u dzieci i młodzieży.
- GINA traktuje łącznie dzieci w wieku od 6 lat, młodzież i dorosłych. Objawy astmy mogą występować do 2 razy w tygodniu lub lek doraźny może być stosowany do 2 razy w tygodniu przed zaobserwowaniem ograniczenia kontroli objawów26.
Ogólne informacje o leczeniu farmakologicznym
- Cel: osiągnięcie optymalnej kontroli astmy
- unikanie obturacji dróg oddechowych
- zmniejszenie nadreaktywności oskrzeli
- wyciszenie zapalenia dróg oddechowych związanego z astmą
- Leczenie farmakologiczne astmy ma na celu osiągnięcie i utrzymanie stanu kontrolowanej astmy zgodnie z zasadą „tyle, ile trzeba, ale jak najmniej”.
- U dzieci i młodzieży należy rozpocząć długotrwałą terapię lekową i dostosować ją tak, aby możliwe było wykonywanie wszystkich codziennych czynności bez leków doraźnych.
- Uzupełnienie leczenia farmakologicznego o środki niefarmakologiczne
- Ważne jest, aby pacjenci mieli jak największą wiedzę na temat swojej choroby i samodzielnego radzenia sobie z nią.
- Zwłaszcza złożone schematy leczenia często prowadzą do braku przestrzegania zasad leczenia.
Leki dzieli się na dwie klasy:
- Leki stosowane długoterminowo („controllers”)
- Długoterminowe leczenie u dzieci i młodzieży jest zalecane, gdy konieczne jest stosowanie leków doraźnych, aby łagodzić objawy astmy utrudniające codzienne funkcjonowanie.
- GKS: Leczenie wziewnymi glikokortykosteroidami (wGKS) stanowi podstawę leczenia długoterminowego.
- Nie zaleca się monoterapii długo działającym LABA lub długo działającym lekiem przeciwcholinergicznym (LAMA).
- Leki doraźne („relievers”)
- SABA: krótko działające beta-2-sympatykomimetyki (SABA) można stosować jako leki doraźne na każdym stopniu intensywności leczenia.
- GINA opowiada się za preferowanym podawaniem GKS + formoterolu w porównaniu do SABA jako lekiem doraźnym, ponieważ przy porównywalnej kontroli objawów można osiągnąć zmniejszone ryzyko zaostrzenia26.
- Niskie zapotrzebowanie na SABA jest ważnym celem i kryterium powodzenia leczenia.
- Alternatywą jest stałe skojarzenie GKS i formoterolu (od 12. roku życia), jeśli stanowi to również leczenie długoterminowe.
- SABA: krótko działające beta-2-sympatykomimetyki (SABA) można stosować jako leki doraźne na każdym stopniu intensywności leczenia.
Drogi podawania leków: wziewna, doustna, pozajelitowa
- Należy preferować podawanie wziewne.
- wyższe stężenia miejscowe, szybszy początek działania i mniej ogólnoustrojowych reakcji niepożądanych
- Leczenie zgodnie ze schematem stopni przyjmowania leków
- Leczenie opiera się na stopniu kontroli astmy.
- Pomimo odpowiedniego leczenia i przestrzegania zasad terapii zdarzają się przypadki, w których nie udaje się osiągnąć dobrej kontroli astmy.
- Leczenie opiera się na stopniu kontroli astmy.
Technika inhalacji i wybór systemu inhalacyjnego
- Wybór systemu inhalacyjnego
- dostosowanie do możliwości poznawczych, motorycznych i wieku pacjentów
- po uzgodnieniu z pacjentami (preferencje)
- w miarę możliwości tylko jeden jednolity system inhalacyjny (tylko jeden typ inhalatora ciśnieniowego dozującego lub proszkowego)
- unikanie zmiany systemu inhalacyjnego w trakcie leczenia (ryzyko błędów w obsłudze)
- po zmianie ponowne wprowadzenie pacjenta do systemu obsługi
- Szkolenie pacjentów w zakresie stosowania systemów inhalacyjnych
- sama informacja na ulotce dołączonej do opakowania zazwyczaj jest niewystarczająca
- demonstracja sposobu działania i w razie potrzeby instrukcje z obrazkami
- regularne sprawdzanie techniki inhalacji (zwłaszcza w przypadku niedostatecznej kontroli astmy)
- Ogólne zasady stosowania systemów inhalacyjnych
- Przed inhalacją
- głęboki wydech (wyjątek: nebulizator)
- Inhalatory ciśnieniowe dozujące należy wstrząsnąć przed użyciem.
- Podczas inhalacji
- optymalny manewr oddechowy zależny od rodzaju systemu inhalacyjnego
- inhalator ciśnieniowy dozujący i nebulizator: możliwie powolny i głęboki wdech
- Inhalator proszkowy: wymuszona inhalacja z jak najsilniejszym przepływem powietrza (nie nadaje się dla małych dzieci lub w przypadku napadu astmatycznego)
- Po inhalacji
- pauza na końcu wdechu trwająca co najmniej 3, a najlepiej 5 sekund
- odstawienie urządzenia (unikanie wydechu do urządzenia)
- Przed inhalacją
- Urządzenia wspomagające inhalację (np. komora inhalacyjna)
- możliwość stosowania od 1. roku życia
- zwiększenie depozycji leku w płucach
- Mogą być pomocne w unikaniu miejscowych reakcji niepożądanych poprzez zmniejszenie depozycji w jamie ustnej27.
- Najbardziej odpowiednie systemy aplikacji dla dzieci:
- dzieci poniżej 5 lat
- preferowane inhalatory zawierające gaz nośnikowy z komorą inhalacyjną
- jak najwcześniejsze zastąpienie maski twarzowej ustnikiem (np. po ukończeniu przez dziecko 2. roku życia)
- dzieci od 5 lat
- inhalator ciśnieniowy dozujący z komorą inhalacyjną i ustnikiem
- Patrz tabela Astma u dzieci i młodzieży, zasadniczo odpowiednie systemy inhalacyjne.
- dzieci poniżej 5 lat
Dawkowanie wziewnych glikokortykosteroidów (wGKS)
Uwaga dotycząca inhalatorów ciśnieniowych dozujących
- Inhalatory ciśnieniowe dozujące wykorzystują propelenty do dostarczenia substancji czynnej do głębokich partii płuc.
- Choć nie niszczą one warstwy ozonowej, są silnymi gazami cieplarnianymi.
- W związku z tym inhalatory ciśnieniowe mają znacznie większy potencjał szkodliwości dla atmosfery w porównaniu z inhalatorami proszkowymi.
- Niemniej jednak inhalatory ciśnieniowe są wskazane w następujących przypadkach:
- u dzieci <5 lat do wziewnego stosowania saba lub gks>
- w przypadku ostrego napadu astmatycznego
- Osoby przepisujące leki, farmaceuci i pacjenci powinni brać pod uwagę, że istnieją znaczne różnice w potencjale globalnego ocieplenia (Global Warming Potential — GWP) pomiędzy poszczególnymi inhalatorami ciśnieniowymi i preferować te o najniższym wskaźniku GWP, jeśli ich skuteczność jest klinicznie porównywalna.
- W przypadku stabilnej astmy od 5. roku życia inne leki wziewne są równie skuteczne jak inhalatory ciśnieniowe.
Leczenie w ostrym napadzie astmatycznym
- Zobacz artykuł Napad astmatyczny u dzieci i młodzieży.
Leki stosowane w ostrym stanie28
- Wprowadzanie przy ostrych objawach i napadzie astmatycznym u dzieci i młodzieży
- SABA
- np. salbutamol lub terbutalina
- najważniejsze leczenie ostrych objawów astmy na wszystkich stopniach intensywności leczenia
- Krótko działające leki przeciwcholinergiczne
- np. bromek ipratropium
- zalecane wprowadzenie w ciężkich i zagrażających życiu napadach astmatycznych oraz w przypadku niewystarczającego działania SABA
- Mogą mieć lepsze działanie w skojarzeniu z SABA niż podawane oddzielnie
- Glikokortykosteroidy doustne (dGKS)
- np. prednizolon
- Wczesne wprowadzenie doustnych glikokortykosteroidów zmniejsza prawdopodobieństwo hospitalizacji29.
- Podawanie tlenu
- W napadzie astmatycznym zaleca się podawanie tlenu z małą szybkością przepływu.
- cel: saturacja O2 >94% u dzieci
- W napadzie astmatycznym zaleca się podawanie tlenu z małą szybkością przepływu.
- Siarczan magnezu
- Dożylne podawanie siarczanu magnezu jest zalecane w przypadku ciężkich napadów astmatycznych ze słabą odpowiedzią na leczenie oraz w przypadku ataków zagrażających życiu30.
- Teofilina
- Spadek liczby recept w ostatnich latach, środek nie ma już znaczenia w leczeniu astmy.
- niski zakres terapeutyczny, możliwość wystąpienia reakcji niepożądanych i dostępne alternatywy
- podawanie jako indywidualna decyzja tylko w sytuacjach zagrożenia życia i przy braku odpowiedzi na początkową terapię
- oznaczanie poziomów w surowicy po pierwszym podaniu
- Spadek liczby recept w ostatnich latach, środek nie ma już znaczenia w leczeniu astmy.
Leczenie długoterminowe28
- Wziewne glikokortykosteroidy (wGKS)
- np. beklometazon, flutikazon, budezonid
- Glikokortykosteroidy wziewne (wGKS) są najskuteczniejszymi dostępnymi lekami do stosowania na stałe31-32.
- Patrz Tabela porównawcza dawkowania wziewnych glikokortykosteroidów (wGKS) u dzieci i młodzieży.
- Potwierdzone efekty
- ograniczenie zapalenia błony śluzowej dróg oddechowych
- zmniejszenie nadreaktywności oskrzeli
- poprawa czynności płuc
- mniejsza częstotliwość objawów astmy, rzadsze i łagodniejsze zaostrzenia
- zmniejszenie ilości leków doraźnych31
- zmniejszenie liczby przyjęć do szpitala i zgonów
- Reakcje niepożądane: mogą wystąpić miejscowe reakcje niepożądane (pleśniawki jamy ustnej, osłabienie głosu).
- Długo działające beta-2-mimetyki (LABA)
- np. formoterol, salmeterol
- Zaleca się wprowadzanie w skojarzeniu z GKS, nie w monoterapii35.
- Cztery badania, w których porównywano leczenie samym GKS z leczeniem skojarzonym GKS i LABA, wykazały:36
- mniej zaostrzeń w przypadku leczenia skojarzonego niż w przypadku stosowania samych GKS
- brak zwiększonego ryzyka poważnych zdarzeń związanych z astmą w przypadku leczenia skojarzonego w porównaniu z monoterapią GKS
- Antagonisty receptora leukotrienowego (LTRA): montelukast
- Montelukast może być stosowany jako monoterapia u dzieci w wieku 2–14 lat na 2 stopniu intensywności leczenia.
- Wprowadzanie jest coraz częściej oceniane krytycznie ze względu na neuropsychiatryczne reakcje niepożądane.
- Montelukast może być stosowany jako terapia dodatkowa, jeśli leczenie GKS nie zapewnia wystarczającej kontroli (tj. na stopniu 4 lub 5 intensywności leczenia).37-40
- Długo działające leki przeciwcholinergiczne (LAMA): tiotropium
- Nie należy stosować leków z grupy LAMA jako monoterapii, a w razie potrzeby jako terapię dodatkową w leczeniu długoterminowym.
- Przeciwciała anty-IgE: omalizumab
- Przeciwciało monoklonalne wiąże się z krążącymi w organizmie przeciwciałami typu IgE.
- Może być stosowany w przypadku ciężkiej astmy, która jest niekontrolowana pomimo optymalnego leczenia31,41.
- zatwierdzony dla dzieci w wieku od 6 lat, młodzieży i dorosłych na stopniu 6 intensywności leczenia
- Bardzo drogie leczenie, które powinno być zlecane przez specjalistów.
- być może zwiększona częstość występowania zdarzeń sercowo-naczyniowych, takich jak zawały serca i zatory płucne
- Przeciwciało przeciwko receptorowi IL-4: dupilumab
- wprowadzanie od 6. roku życia u osób z zapaleniem astmatycznym typu 2
- ampułko-strzykawka w dawce 200 lub 300 mg do wstrzykiwań podskórnych
- Przy pierwszym użyciu u młodzieży i dorosłych wstrzykuje się łącznie 400 lub 600 mg substancji czynnej za pomocą dwóch strzykawek, w zależności od innych leków na astmę.
- Następnie kontynuuje się leczenie za pomocą jednej strzykawki co dwa tygodnie (200–300 mg).
- Po przeszkoleniu przez lekarza pacjenci mogą również samodzielnie wykonywać zastrzyki.
- Przeciwciało przeciwko receptorowi IL-5: mepolizumab
- Przeciwciała anty-IL-5 jako leczenie dodatkowe zmniejszają liczbę zaostrzeń u pacjentów z ciężką, źle kontrolowaną astmą eozynofilową o ok. 50 %.42
- mepolizumab zatwierdzony jako przedstawiciel tej grupy dla dzieci w wieku 6 lat i starszych
- Korzyści ze stosowania mepolizumabu w ciężkiej astmie opornej na leczenie stwierdzono jedynie w przypadku liczby eozynofili we krwi wynoszącej co najmniej 150/mcl. Największe korzyści odnoszą pacjenci z liczbą eozynofili 500/mcl i wyższą.
- Mepolizumab jest preferowany w stosunku do dupilumabu i tezepelumabu ze względu na wyższy poziom przetestowania, potwierdzone potencjalne oszczędności na dGKS i niższy koszt.
- Przeciwciało przeciwko limfopoetynie zrębu limfatycznego: tezepelumab
- wprowadzanie od 12. roku życia jako dodatkowe leczenie podtrzymujące przy ciężkiej astmie
- Zalecana dawka wynosi 210 mg tezepelumabu we wstrzyknięciu podskórnym co 4 tygodnie.
Stopniowy schemat leczenia farmakologicznego u dzieci i młodzieży
- Patrz tabela Stopnie intensywności farmakologicznego leczenia astmy u dzieci i młodzieży.
- GINA nie zaleca już monoterapii SABA u młodzieży i dorosłych, ale zawsze w skojarzeniu z wziewnymi glikokortykosteroidami (wGKS). Ogólnie rzecz biorąc, wszyscy dorastający i dorośli pacjenci z astmą powinni otrzymywać GKS26.
- Powodem tego jest przypuszczalny wzrost ryzyka zaostrzeń przy monoterapii SABA.
- w przypadku łagodnej astmy stała kombinacja GKS + formoterol również jako lek doraźny
Leczenie początkowe u dzieci i młodzieży
- W przypadku kryteriów częściowo kontrolowanej astmy długoterminowe leczenie należy zwykle rozpoczynać na stopniu 2 intensywności leczenia.
- W przypadku kryteriów niekontrolowanej astmy długoterminowe leczenie należy rozpocząć co najmniej na stopniu 3 intensywności leczenia.
Stopień 1 intensywności leczenia u dzieci i młodzieży
- Leczenie doraźne
- SABA
- SABA jako lek doraźny dla pacjentów z łagodnymi lub rzadkimi objawami
- np. salbutamol 1–2 dawki z inhalatora ciśnieniowego (maks. 6 dawek dziennie u dzieci)
- Rozwiązanie alternatywne w uzasadnionych przypadkach (reakcje niepożądane lub przeciwwskazania do stosowania SABA)
- bromek ipratropium jako dodatek lub alternatywa dla SABA
- Od 12. roku życia: stałe skojarzenie małej dawki GKS + formoterolu
- SABA
- Według GINA istnieje zwiększone ryzyko zaostrzeń przy zastosowaniu samej terapii SABA26.
- Dlatego nie powinno się już tego zalecać młodzieży i dorosłym.
- Według GINA niezatwierdzone w naszym kraju GKS powinny być podawane wziewnie w razie potrzeby w połączeniu z szybko, ale jednocześnie długo działającym LABA (budezonid plus formoterol).
- W przypadku konieczności stosowania leków doraźnych w celu umożliwienia wykonywania codziennych czynności bez objawów astmy:
- zalecane długotrwałe leczenie przeciwzapalne za pomocą wGKS (stopień 2 intensywności leczenia)
Stopień 2 intensywności leczenia u dzieci i młodzieży
- Leczenie doraźne
- wziewny SABA
- np. salbutamol 1–2 dawki z inhalatora ciśnieniowego (maks. 6 dawek dziennie u dzieci)
- Rozwiązanie alternatywne w uzasadnionych przypadkach (reakcje niepożądane lub przeciwwskazania do stosowania SABA)
- bromek ipratropium jako dodatek lub alternatywa dla SABA
- wziewny SABA
- Leczenie długoterminowe
- preferowany wGKS w małej dawce
- np. beklometazon 100–200 mcg/dobę
- podawany jako pojedyncza dawka lub podzielony na 2 dawki dzienne
- w razie potrzeby zastosowanie urządzeń wspomagających inhalację (komory inhalacyjnej)
- rozwiązanie alternatywne w uzasadnionych przypadkach
- od 12. roku życia: w zależności od potrzeb stosowanie stałego skojarzenia wGKS w małej dawce + formoterolu (leczenie poza wskazaniami rejestracyjnymi)
- W takim przypadku nie jest konieczne dalsze leczenie doraźne przy użyciu SABA.
- LTRA montelukast jako monoterapia
- w przypadku wystąpienia reakcji niepożądanych lub przeciwwskazań do stosowania wGKS
- Nie zaleca się stosowania u pacjentów w wieku powyżej 15. roku życia, chyba że nie są w stanie przyjmować wziewnie wGKS lub wystąpią u nich nieakceptowalne reakcje niepożądane.
- preferowany wGKS w małej dawce
Stopień 3 intensywności leczenia u dzieci i młodzieży
- Leczenie doraźne
- SABA
- np. salbutamol 1–2 dawki z inhalatora ciśnieniowego (maks. 6 dawek dziennie u dzieci)
- Rozwiązanie alternatywne w uzasadnionych przypadkach (reakcje niepożądane lub przeciwwskazania do stosowania SABA)
- bromek ipratropium jako dodatek lub alternatywa dla SABA
- SABA
- Leczenie długoterminowe
- wGKS w średniej dawce
- np. beklometazon 200–400 mcg/dobę
- Należy zaczynać od dolnej dawki średnio wysokiej.
- wGKS w średniej dawce
Stopień 4 intensywności leczenia u dzieci i młodzieży
- Skierowanie do specjalisty pneumologii dziecięcej
- Leczenie doraźne
- SABA
- np. salbutamol 1–2 dawki z inhalatora ciśnieniowego (maks. 6 dawek dziennie u dzieci)
- Stałe skojarzenie wGKS i LABA (formoterolu), jeśli jest to również stosowane leczenie długoterminowe.
- u młodzieży od 12. roku życia
- rozwiązanie alternatywne w uzasadnionych przypadkach (reakcje niepożądane lub przeciwwskazania do stosowania SABA)
- bromek ipratropium jako dodatek lub alternatywa dla SABA
- SABA
- Leczenie długoterminowe
- skojarzenie wGKS w średniej dawce i LABA
- np. salmeterol/flutykazon 25 mcg/50 mcg w inhalatorze ciśnieniowym dozującym 2 razy 1–2 wdechy/dobę u dzieci w wieku od 4 lat
- skojarzenie wGKS w średniej dawce i LTRA
- skojarzenie wGKS w średniej dawce, LABA i LTRA
- rozwiązanie alternatywne w przypadku nieuzyskania wystarczającej kontroli przy skojarzeniu trzech leków:
- skojarzenie wGKS w średniej dawce, LABA i LTRA oraz LAMA
- niższe ryzyko reakcji niepożądanych niż w przypadku zwiększania dawki wGKS
- skojarzenie wGKS w średniej dawce i LABA
Stopień 5 intensywności leczenia u dzieci i młodzieży
- Przed przejściem/przy przejściu do stopnia 5
- ocena skuteczności różnych możliwych opcji leczenia ze stopnia 4
- ze względu na obawy związane z bezpieczeństwem wyższego dawkowania wGKS
- badanie wskazań do rehabilitacji w warunkach szpitalnych
- leczenie kontrolowane (przestrzeganie zaleceń) i trening zachowań
- skierowanie do specjalisty pneumologii dziecięcej i wizyta w centrum pneumologii dziecięcej w celu wykonania rozszerzonej diagnostyki
- ocena skuteczności różnych możliwych opcji leczenia ze stopnia 4
- Leczenie doraźne
- leczenie doraźne jak w stopniu 4
- Opcje leczenia długoterminowego
- skojarzenie wGKS w wysokiej dawce i LABA
- np. salmeterol/flutykazon 25 mcg/50 mcg w inhalatorze ciśnieniowym dozującym 2 razy 1–2 wdechy/dobę u dzieci w wieku od 4 lat
- skojarzenie wGKS w wysokiej dawce, LABA i LAMA
- skojarzenie wGKS w wysokiej dawce i LTRA
- skojarzenie wGKS w wysokiej dawce, LABA i LTRA
- skojarzenie wGKS w wysokiej dawce, LABA i LTRA oraz LAMA
- skojarzenie wGKS w wysokiej dawce i LABA
Stopień 6 intensywności leczenia u dzieci i młodzieży
- Przed przejściem/przy przejściu do stopnia 6
- ocena skuteczności różnych możliwych opcji leczenia ze stopnia 5
- wizyta w centrum pneumologii dziecięcej z możliwością wykonania diagnostyki inwazyjnej
- wykluczenie rozpoznań różnicowych i chorób współistniejących o większym znaczeniu przed leczeniem przeciwciałami monoklonalnymi lub dGKS
- badanie wskazań do rehabilitacji w warunkach szpitalnych
- Leczenie doraźne
- leczenie doraźne jak w stopniu 4
- Leczenie długoterminowe
- Dodatkowo przeciwciała anty-IgE (omalizumab przez co najmniej 4 miesiące) u dzieci w wieku 6 lat i starszych, jeśli występują następujące kryteria:
- ciężka astma alergiczna IgE-zależna — i —
- dodatni wynik testu skórnego lub reaktywność in vitro na występujący całorocznie alergen wziewny — i —
- stężenie IgE w surowicy z uwzględnieniem masy ciała w zakresie umożliwiającym leczenie — i —
- eliminacja możliwych do uniknięcia ekspozycji na alergeny
- alternatywnie przeciwciała przeciwko receptorowi IL-4 lub przeciwciała przeciwko receptorowi IL-5
- Określenie wskazań i rozpoczęcie leczenia przeciwciałami monoklonalnymi u dzieci i młodzieży powinny być prowadzone przez pulmonologów dziecięcych z doświadczeniem w leczeniu ciężkiej astmy.
- Z grupy przeciwciał anty-IL-4-R dupilumab jest zatwierdzony od 6. roku życia.
- Z grupy przeciwciał anty-IL-5 mepolizumab jest zatwierdzony do leczenia astmy od 6. roku życia.
- od 12. roku życia dodatkowe przeciwciało przeciwko limfopoetynie zrębu grasicy (tezepelumab) jako opcja
- Dodatkowo przeciwciała anty-IgE (omalizumab przez co najmniej 4 miesiące) u dzieci w wieku 6 lat i starszych, jeśli występują następujące kryteria:
- Rozwiązanie alternatywne w uzasadnionych przypadkach
- dGKS
- ostatnia opcja leczenia dla dzieci i młodzieży po wyczerpaniu wszystkich innych środków
- długotrwała terapia dGKS z ryzykiem poważnych reakcji niepożądanych: dokładne wyjaśnienie i ocena przebiegu leczenia
- podawanie w najmniejszej skutecznej dawce
- Stosowanie tylko wtedy, gdy kontrola astmy jest niewystarczająca pomimo skojarzenia różnych metod leczenia z poprzedniego stopnia oraz dodatkowo przeciwciał monoklonalnych.
- przy długotrwałym leczeniu profilaktyka osteoporozy
- dGKS
Kontrola leczenia
Aspekty bezpieczeństwa w dzieciństwie i okresie dojrzewania
- W przypadku długotrwałego leczenia wGKS
- ustawienie najniższej skutecznej dawki
- regularna kontrola wzrostu z zapisem w krzywej wzrostu
- przy podejrzeniu supresji nadnerczy: diagnostyka lub leczenie
Dostosowanie terapii ukierunkowanej na kontrolę astmy
- Astma kontrolowana
- Należy zastanowić się nad redukcją terapii (patrz schemat stopniowy).
- Astma powinna być kontrolowana przez co najmniej 3 miesiące przed ewentualną redukcją terapii za pomocą ICS.
- Nie dotyczy to pacjentów z astmą sezonową. Tutaj leczenie jest ukierunkowane na sezonowe narażenie na pyłki, dzięki czemu redukcja jest możliwa już po krótszym czasie.
- Ponieważ unikanie nadmiernego leczenia jest szczególnie istotne w dzieciństwie, przy stabilnej kontroli astmy można ewentualnie podjąć próbę redukcji leczenia już po 2 miesiącach.
- Zaleca się ścisłe monitorowanie w przypadku przerwania terapii kortykosteroidami lub przeciwciałami monoklonalnymi.
- Astma częściowo kontrolowana lub niekontrolowana
- sprawdzenie techniki inhalacji (demonstracja przez pacjenta) i adherencji terapeutycznej
- przegląd potrzeb szkoleniowych
- kontrola alergii i środowiska
- uwzględnienie chorób współistniejących i czynników obciążających
- weryfikacja rozpoznania astmy
- Astma częściowo kontrolowana
- Należy rozważyć intensyfikację leczenia (patrz schemat stopni).
- Astma niekontrolowana
- Zaleca się intensyfikację leczenia (patrz schemat stopni).
- Obserwacja, ponowna wizyta (po intensyfikacji w ciągu 3 miesięcy)
Inne opcje leczenia
Immunoterapia (alergenowo) swoista w astmie alergicznej (specific immunotherapy — SIT)
- Zobacz także artykuł Immunoterapia alergenowo swoista (SIT).
- wczesne wprowadzenie u dzieci z kontrolowaną alergiczną astmą oskrzelową IgE-zależną z wyraźnym wykazaniem odpowiedzialnego alergenu
- dwie formy
- immunoterapia podskórna (subcutaneous immunotherapy — SCIT)
- immunoterapia podjęzykowa (sublingual immunotherapy — SLIT)
- SIT zmniejsza objawy i zapotrzebowanie na leki u dzieci z alergiami43-44.
- Może zmniejszać ryzyko rozwoju astmy u dzieci z alergicznym nieżytem nosa i spojówek44-45.
- Wskazanie do stosowania SIT w przynajmniej częściowo kontrolowanej astmie alergicznej IgE-zależnej powinno być rozważane jako opcja leczenia obok unikania alergenów i leczenia farmakologicznego.
- Wymagania
- jednoznaczny związek przyczynowy między objawami oddechowymi a odpowiadającemu im narażeniu na alergen
- potwierdzenie odpowiadającego uczulenia swoistego dla alergenu
- Wprowadzenie preparatów, których skuteczność u pacjentów z astmą została potwierdzona w kontrolowanych badaniach klinicznych.
- Określenie wskazania i dobór antygenów oraz formy podania przez lekarza specjalizującego się w alergologii
- Nie zastępuje terapii przeciwastmatycznej.
- określenie wskazania bardziej restrykcyjne niż w przypadku alergicznego nieżytu nosa i spojówek
- Dwie formy
- immunoterapia podskórna (subcutaneous immunotherapy — SCIT)
- immunoterapia podjęzykowa (sublingual immunotherapy — SLIT)
- Przeciwwskazania: niekontrolowana astma i/lub FEV1 <70% wartości docelowej>
Niefarmakologiczne sposoby postępowania przy astmie
- Leczenie farmakologiczne astmy powinno być regularnie uzupełniane o niefarmakologiczne działania lecznicze.
- Celem jest między innymi poprawa umiejętności radzenia sobie z chorobą i samodzielnej kontroli.
- Do środków niefarmakologicznych w przypadku astmy należą:
- edukacja pacjentów i usługi informacyjne
- fizjoterapia i fizjoterapia układu oddechowego
- aktywność fizyczna
- unikanie narażenia na alergeny lub inne czynniki wyzwalające
- redukcja masy ciała przy otyłości
- w razie potrzeby rzucenie palenia
- w razie potrzeby poradnictwo społeczne i zawodowe
- wsparcie ze strony rodziny i społeczności
Usługi informacyjne i edukacja pacjentów
- Wszystkim pacjentom z astmą, którzy są długotrwale leczeni farmakologicznie, należy zalecić i umożliwić udział w zorganizowanym programie treningu zachowań46.
- W przypadku dzieci i młodzieży należy w miarę możliwości zaangażować rodziców.
- Należy zapewnić regularne szkolenia uzupełniające.
- Potwierdzone działanie
- poprawa kontroli astmy z mniejszą liczbą napadów astmatycznych
- poprawa jakości życia
- zmniejszenie liczby dni hospitalizacji, niezdolności do pracy i nieobecności w szkole
- aktywny udział pacjentów (w przypadku dzieci i młodzieży także ich rodzin) w procesie radzenia sobie z chorobą
- Treść programów edukacyjnych
- patofizjologia i czynniki wyzwalające chorobę
- zasady leczenia
- techniki inhalacji
- przestrzeganie schematu leczenia
- zdolność do samokontroli
- indywidualny plan działania w przypadku astmy lub plan samodzielnej kontroli
- np. dzienniczek objawów, domowe pomiary PEF
- samodzielne dostosowanie leczenia
- np. plan awaryjny w sytuacji wstępnego samodzielnego leczenia
Unikanie czynników wyzwalających
- W miarę możliwości należy unikać zidentyfikowanych czynników wyzwalających, np. zimnego powietrza czy zanieczyszczeń powietrza.
- niestosowanie leków potencjalnie wywołujących napady (ASA, NLPZ lub beta-blokerów)
- Unikanie alergenów
- podstawa leczenia astmy alergicznej
- Adaptacja środowiska domowego
- Unikanie wilgotnego klimatu w pomieszczeniach i miejsc, gdzie rozwija się pleśń.
- środki zmniejszające narażenie na alergeny, np. specjalne pokrowce na łóżka chroniące przed roztoczami kurzu domowego lub filtry powietrza47-49
- Krajowe Wytyczne Ochrony Zdrowia oceniają odporne na roztocza ochraniacze na materace jako środek, który może potencjalnie przyczynić się do redukcji alergenów.
Fizjoterapia
- Fizjoterapia oddechowa
- mobilizacja mięśni oddechowych oraz nauka i wzmocnienie fizjologicznych wzorców oddechowych
- Powinna być proponowana wszystkim pacjentom, u których współwystępuje astma i zaburzenia oddychania (także DSG).
- Powinna być zalecana pacjentom z astmą i potrzebą dodatkowego leczenia lub lękiem wywołanym przez duszność.
- Celem jest kontrolowanie duszności, podrażnienia wywołującego kaszel i niepokoju.
- Trening oddechowy połączony z treningiem relaksacyjnym lub metodami biofeedback może również prowadzić do zmniejszenia objawów i poprawy jakości życia50.
Aktywność fizyczna
- Wszystkim pacjentom z astmą należy zalecić trening fizyczny (np. wychowanie fizyczne w szkole, ćwiczenia wspomagające płuca).
- Objawy wywołane wysiłkiem fizycznym są często wyrazem niedostatecznej kontroli astmy.
- w razie potrzeby intensyfikacja leczenia długoterminowego zgodnie z zasadami stopni intensywności leczenia
- Efekty regularnej aktywności fizycznej to:51
- zmniejszenie objawów astmy
- poprawa odporności
- poprawa jakości życia
- zmniejszenie zachorowalności
- uniknięcie stygmatyzacji
- Przy astmie i otyłości zalecana jest redukcja masy ciała.
- Metody służące redukcji masy ciała muszą zostać trwale zaplanowane i obejmować aktywność fizyczną.
Rehabilitacja
- Może być przydatna w przypadku częściowo kontrolowanej lub niekontrolowanej astmy, aby umożliwić normalne uczestnictwo w życiu codziennym.
- Działania rehabilitacyjne należy rozważyć zwłaszcza po napadach astmatycznych leczonych w warunkach szpitalnych.
- Podejście multimodalne obejmuje m.in:
- spersonalizowaną diagnostykę
- badanie czynników wyzwalających i narażenia na alergeny
- optymalizację leczenia
- edukowanie pacjentów
- fizjoterapię i terapię treningową
- poradnictwo psychologiczne i psychoterapię
- rzucenie palenia
- konsultacje dietetyczne
- doradztwo zawodowe
Astma i choroby współistniejące
- Nieżyt nosa
- Astma związana jest z przewlekłymi chorobami zapalnymi górnych dróg oddechowych.
- Niektórzy autorzy uważają, że choroby zapalne o takiej samej patogenezie w górnych i dolnych drogach oddechowych stanowią jednolity obraz kliniczny (hipoteza „united airways”).
- Przewlekłe choroby zapalne górnych dróg oddechowych powinny być rzetelnie rozpoznawane i leczone, aby zapobiec rozwojowi lub pogorszeniu astmy oskrzelowej.
- Refluks
- Refluks żołądkowo-przełykowy występuje znacznie częściej u pacjentów z astmą, niż u zdrowej populacji.
- Objawowa choroba refluksowa powinna być leczona.
- Jednak leczenie hamujące wydzielanie kwasu nie poprawia przebiegu astmy u dzieci z objawami refluksu lub bez nich52-53.
- Choroby psychiczne
- Szczególnie często jednocześnie z astmą występują zaburzenia lękowe i depresja.
- Są one niedostatecznie diagnozowane i mogą komplikować leczenie i samodzielną kontrolę choroby.
- U dzieci i młodzieży rozwój fizyczny, umysłowy i edukacyjny może być zaburzony przez współistniejące choroby psychiczne.
- Leczenie psychospołeczne i psychoterapeutyczne stanowi często część rehabilitacji pneumologicznej54.
Terapia komplementarna
- Pacjentów (a w przypadku dzieci — ich rodziców) należy zapytać, czy stosują alternatywne lub komplementarne metody leczenia astmy, a jeśli tak, to należy poinformować ich o ryzyku z tym związanym.
- W związku z niewystarczającą ilością danych nie można sformułować wiarygodnego stwierdzenia na temat poniższych metod lub ze względu na niewystarczającą skuteczność bądź jej brak w różnych badaniach nie można wydać dla nich zalecenia:
- akupunktura
- homeopatia
- chiropraktyka
- działania związane z dietą (olej rybny, ograniczenie soli, podawanie witaminy C, suplementacja lub ograniczenie spożycia minerałów)
- hipnoza lub techniki relaksacyjne
- jonizatory powietrza w pomieszczeniach mieszkalnych (air ionizers)
- kontrola wilgotności powietrza
- speleoterapia
- tradycyjna medycyna chińska
- fitoterapeutyki
- termoplastyka oskrzela
- U pacjentów z niekontrolowaną astmą i częstymi zaostrzeniami należy oznaczyć poziom witaminy D i w razie potrzeby wprowadzić suplementy witaminy D.
- U niektórych pacjentów z niskim poziomem witaminy D i częstymi napadami astmatycznymi, którzy muszą być leczeni ogólnoustrojowymi glikokortykosteroidami, może to zapobiegać kolejnym napadom astmatycznym.
- Ponadto nie ma danych na temat poważnych reakcji niepożądanych.
Zalecenia dla pacjentów
- Nauka samodzielnej kontroli choroby
- nauka prawidłowych technik inhalacji
- rozpoznawanie znaków ostrzegawczych napadu astmatycznego
- Prowadzi do zmniejszenia zachorowalności i zapotrzebowania na opiekę medyczną46.
- Aktywność fizyczna
- Należy zachęcać dzieci do aktywności fizycznej, ponieważ ma to korzystny wpływ na przebieg choroby.
- Celem jest normalne uczestnictwo w zajęciach sportowych.
- U nastolatków pływanie jest zwykle dobrze tolerowane; może ono poprawić czynność płuc55.
- W przypadku ostrego napadu astmatycznego
- Podczas napadu astmatycznego dziecko nie powinno pozostawać bez opieki.
- Zapewnić spokojne otoczenie, w którym dziecko może przyjąć wygodną pozycję.
- Jeśli napad jest łagodny, a pacjent ma dobrą wiedzę na temat choroby, leczenie można przeprowadzić samodzielnie.
Wybór zawodu w przypadku młodzieży z astmą
- Aby dać młodym ludziom wystarczająco dużo czasu na rozważenie odpowiedniego wyboru kariery zawodowej, proces doradztwa nie powinien rozpoczynać się dopiero po zakończeniu szkoły. Wstępne wskazania powinny być raczej podawane w kontekście opieki pediatrycznej, jeszcze zanim zostaną ugruntowane aspiracje zawodowe.
- Ogólnie rzecz biorąc, sama obecność uczulenia alergicznego na powszechne alergeny powietrznopochodne i nieswoista nadreaktywność oskrzeli są związane ze zwiększonym prawdopodobieństwem ponownego wystąpienia astmy, ale nie są wystarczające jako jedyne kryterium decyzyjne.
- Jeśli to możliwe, okres próbny powinien być traktowany jako staż, kurs kształcenia podstawowego, kurs wyrównawczy, rok przygotowania zawodowego lub zasadniczy rok kształcenia zawodowego, w zależności od oferty.
- Jedynie nastolatkom cierpiącym na ciężką astmę należy odradzać wykonywanie zawodu o profilu ryzyka związanym z astmą.
- Zawody o wysokim profilu ryzyka obejmują m.in.:
- zawody związane z przetwórstwem mąki, ogrodnictwo, florystykę, stolarstwo, weterynarię, kosmetologię, technikę dentystyczną, lakiernictwo, gospodarkę odpadami
Zapobieganie
Informacje ogólne
- Zobacz także artykuł Zapobieganie alergii.
- Jeśli to możliwe, przez pierwsze 4–6 miesięcy dziecko należy karmić wyłącznie piersią.
- W zależności od gotowości niemowlęcia do rozszerzenia diety należy je rozpocząć najwcześniej od początku 5. miesiąca życia, a najpóźniej od początku 7. miesiąca życia.
- Należy unikaćnadwagi/otyłości u kobiet przed ciążą i w jej trakcie oraz u dzieci i młodzieży w związku z zapobieganiem astmie.
- Niektóre badania pokazują, że niski poziom długołańcuchowych kwasów tłuszczowych omega-3 u kobiet w ciąży, matek karmiących piersią i niemowląt wiąże się z wyższym ryzykiem chorób alergicznych u dziecka, zwłaszcza astmy i świszczącego oddechu, oraz że ryzyko to można zmniejszyć poprzez suplementację długołańcuchowych kwasów tłuszczowych omega-3.
- Osoby bez rozpoznawalnego zwiększonego ryzyka alergii nie powinny ograniczać posiadania zwierząt domowych do kotów lub psów.
- Rodziny ze zwiększonym ryzykiem alergii lub posiadające dzieci, które już mają wyprysk atopowy nie powinny nabywać nowego kota.
- Wszystkie dzieci powinny być szczepione zgodnie z aktualnymi zaleceniami.
- Podczas udzielania porad dotyczących sposobu porodu należy wziąć pod uwagę, że dzieci urodzone przez cesarskie cięcie mają nieznacznie zwiększone ryzyko astmy.
- W przypadku wprowadzenia antybiotyków w okresie niemowlęcym, należy wziąć pod uwagę, że przyjmowanie antybiotyków przez dziecko w pierwszych dwóch latach życia wiąże się ze średnim wzrostem ryzyka wystąpienia astmy alergicznej i niewielkim wzrostem ryzyka wystąpienia kataru siennego oraz egzemy w późniejszym okresie życia. W przypadku stosowania antybiotyków w ciąży należy wziąć pod uwagę, że przyjmowanie ich przez matkę w czasie ciąży wiąże się ze średnim wzrostem ryzyka rozwoju astmy u dziecka w późniejszym okresie życia.
- Należy unikać czynnego i biernego narażenia na dym tytoniowy. Ta zasada obowiązuje już w okresie ciąży.
- Należy unikać warunków w pomieszczeniach, które sprzyjają rozwojowi pleśni (wysoka wilgotność, brak wentylacji).
- Narażenie na emisje związane z pojazdami silnikowymi i zanieczyszczenie powietrza w pomieszczeniach powinny być utrzymywane na niskim poziomie.
- Telemedycyna może nabrać większego znaczenia w opiece nad pacjentami z astmą.
- Przykładem mogą być systemy przypominania SMS, aplikacje na smartfony i tablety lub działania oparte na grach dla młodzieży.
Immunoterapia swoista (SIT)
- Nie zastępuje leczenia astmy, ale może być stosowana we wczesnym okresie leczenia astmy alergicznej.
- Immunoterapia swoista dla alergenu (SIT, odczulanie) zmniejsza objawy astmy, zapotrzebowanie na leki i swoistą dla alergenu nadreaktywność oskrzeli56.
- Pacjentom z istniejącym alergicznym nieżytem nosa/nieżytem nosa i spojówek należy zalecić immunoterapię swoistą dla alergenu, aby zapobiec jeszcze nie wykształconej astmie.
- Wskazania do działania zapobiegawczego
- U pacjentów z alergicznym nieżytem nosa immunoterapia podskórna zmniejszyła rozwój objawów astmy (zmiana stopnia) do 7 lat po zakończeniu 3-letniego okresu leczenia. 57
Szczepienia
- Astma, podobnie jak inne choroby przewlekłe, zwiększa ryzyko zachorowania na grypę i zakażenia pneumokokowe.
- Pacjentom z astmą należy więc zaproponować szczepienia zgodnie z aktualnymi zaleceniami.
Przebieg, powikłania i rokowanie
Przebieg
- Zapalenie dróg oddechowych powoduje nawracające epizody duszności, ucisku w klatce piersiowej i kaszlu.
- Przebieg choroby może ulegać dużym wahaniom, zwłaszcza jeśli występuje sezonowy komponent alergiczny.
- Liczba przyjęć do szpitala z powodu napadów astmatycznych obecnie wyraźnie maleje (efekt długotrwałego leczenia wGKS).
- Dzieci z wirusowymi zakażeniami układu oddechowego jako czynnikiem wyzwalającym objawy astmy zwykle lepiej radzą sobie latem ze względu na rzadziej występujące zakażenia.
Powikłania
- Ciężki i zagrażający życiu napad astmatyczny
- Śmiertelność wśród dzieci w wieku 0–14 lat zmniejszyła się z biegiem czasu i jest obecnie bardzo niska w Europie.
- Przejście do postaci mieszanej z przewlekłą obstrukcyjną chorobą płuc (zespół nakładania astmy i POChP, ACOS)
- Aspekty bezpieczeństwa długotrwałego leczenia wGKS u dzieci i młodzieży
- ustawienie najniższej skutecznej dawki
- wtórna niewydolność kory nadnerczy58
- szczególnie u pacjentów przyjmujących wziewne glikokortykosteroidy w dużych dawkach (zwłaszcza flutikazon) przez dłuższy czas i ewentualnie ogólnoustrojowe glikokortykosteroidy
- znaki ostrzegawcze to utrata masy ciała, zmęczenie, nudności i wymioty
- opóźnienie rozwoju i wzrostu u dzieci leczonych glikokortykosteroidami
- regularna kontrola wzrostu z zapisem w krzywej wzrostu
- Zwiększone ryzyko zachorowania na grypę i zakażenia pneumokokowe
Rokowanie
- U dużej części dzieci i młodzieży z astmą objawy ustępują w ciągu życia.
- W okresie dojrzewania objawy ulegają poprawie, zwłaszcza u chłopców1.
- U starszych dzieci objawy mają tendencję do zmniejszania się wraz z wiekiem, ale często występują jeszcze w dorosłym życiu59.
- Czynnikami predykcyjnymi uporczywej astmy są atopia, zmniejszona czynność płuc i nadreaktywność oskrzeli.
- Wiek w momencie wystąpienia choroby
- Rokowanie wydaje się być związane z wiekiem w momencie wystąpienia choroby. W szczególności późny początek choroby w wieku dorosłym zwiększa ryzyko pogorszenia czynności płuc i zaostrzeń60.
- Dzieci z łagodną astmą mają dobre rokowanie61.
- Ciężka astma jest często związana ze zwiększonym ryzykiem rozwoju przewlekłej obturacyjnej choroby płuc, zwłaszcza jeśli pacjenci palą.
- Wpływ astmy dziecięcej na życie społeczne i zawodowe (np. edukację) jest w większości przypadków stosunkowo niewielki59.
Dalsze postępowanie
- Stałe monitorowanie i ocena postępu
- zapewnienie długoterminowej kontroli astmy i wybór najniższego skutecznego stopnia intensywności leczenia
- Aby uzyskać informacje na temat dostosowania stopni intensywności leczenia, patrz Dostosowanie leczenia.
- Monitorowanie przebiegu jest wskazane także w przypadku astmy kontrolowanej, ponieważ choroba może ulegać wahaniom.
- zapewnienie długoterminowej kontroli astmy i wybór najniższego skutecznego stopnia intensywności leczenia
- Monitorowanie wzrostu u dzieci i młodzieży z wykorzystaniem siatki centylowej podczas długotrwałego leczenia wGKS
- Szczepienia zgodnie z ogólnymi zaleceniami
- Przy każdej kontroli przebiegu należy ocenić następujące parametry:
- objawy astmy w ciągu dnia, w nocy i podczas wysiłku fizycznego
- częstotliwość stosowania leków doraźnych
- ograniczenia w wykonywaniu czynności życia codziennego
- Adherencja terapeutyczna i technika inhalacji
- częstotliwość występowania i czynniki wyzwalające zaostrzenia
- skuteczność i tolerancja leczenia farmakologicznego
Koordynacja opieki
- Zalecana jest długoterminowa opieka i prowadzenie dokumentacji w ramach ustrukturyzowanego programu leczenia.
- zazwyczaj przez lekarzy rodzinnych lub pediatrów i lekarzy zajmujących się młodzieżą
- w szczególnych przypadkach (trwale wysoka niestabilność lub ciężki przebieg choroby) przez pneumologów dziecięcych
- Jeśli stan się ustabilizuje, konieczne jest dalsze leczenie przez lekarza rodzinnego lub pediatrę.
- Wskazania do skierowania do specjalisty lub hospitalizacji — patrz sekcja Wskazania do skierowania do specjalisty/hospitalizacji.
- Celem skierowania nie jest przede wszystkim zapewnienie długoterminowego leczenia, lecz ocena i, w razie potrzeby dostosowanie leczenia.
- Po każdej hospitalizacji: należy sprawdzić wskazania do zastosowania środka rehabilitacyjnego u dzieci i młodzieży wdrażane bezpośrednio po leczeniu.
- Po napadzie astmatycznym należy niezwłocznie zgłosić się ponownie do lekarza, a ten wdroży następujące środki.
- identyfikacja czynników ryzyka pogorszenia kontroli astmy
- przekazanie lub weryfikacja planu działania w przypadku astmy
- zainicjowanie szkolenia albo szkoleń uzupełniających
- rozważenie potrzeby intensyfikacji leczenia długoterminowego
- sprawdzenie wskazania do rehabilitacji
- Według Światowej Inicjatywy na Rzecz Zwalczania Astmy (The Global Initiative for Asthma — GINA) diagnostyka czynności płuc jest najważniejszym parametrem długoterminowego ryzyka. Badanie należy wykonać w momencie rozpoznania choroby, po 3–6 miesiącach od rozpoczęcia leczenia, a następnie powtarzać w regularnych odstępach czasu, co najmniej raz w roku26.
Możliwe pytania w ramach monitorowania przebiegu
- Patrz tabela Astma u dzieci i młodzieży — pytania kontrolne.
Informacje dla pacjentów
O czym należy poinformować pacjentów?
- Samokontrola, również w przypadku ostrych dolegliwości
- indywidualny plan działania w przypadku astmy lub plan samodzielnej kontroli
- w razie potrzeby zapisy w dzienniku i w uzasadnionych przypadkach pomiary PEF
- Zalecenie szkoleń i przekazanie informacji dla pacjentów i ich rodzin
- Udzielenie wskazówek dotyczących prawidłowej techniki inhalacji
- Możliwość wsparcia ze strony organizacji samopomocowych dla pacjentów
Informacje dla pacjentów w Deximed
Ilustracje
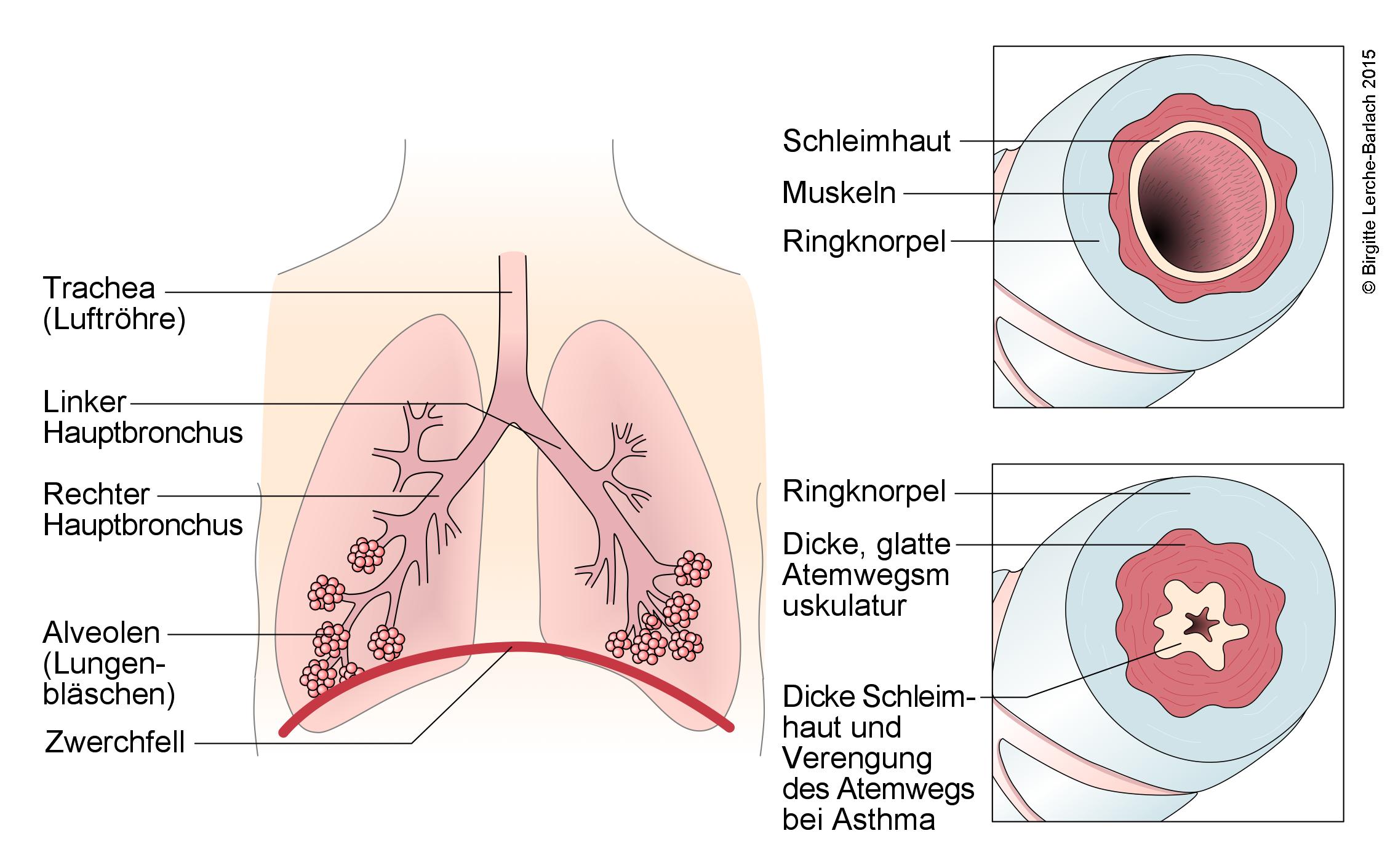
Drogi oddechowe i zmiany w astmie oskrzelowej
Quellen
Leitlinien
- Global Initiative for Asthma (GINA). Pocket Guide for Asthma Management and Prevention. Stand 2022. www.ginasthma.com
Literatur
- Gibson GJ, Loddenkemper R, Sibille Y, et al. (Hrsg) (2013). The European lung white book. Respiratory health and disease in Europe. European Respiratory Society, Sheffield. www.ncbi.nlm.nih.gov
- GBD 2015 Chronic Respiratory Disease Collaborators. Global, regional, and national deaths, prevalence, disability-adjusted life years, and years lived with disability for chronic obstructive pulmonary disease and asthma, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015. Lancet Respir Med. 2017 Sep;5(9):691-706. pubmed.ncbi.nlm.nih.gov
- Ramsey CD, Celedón JC. The hygiene hypothesis and asthma. Curr Opin Pulm Med. 2005 Jan;11(1):14-20. Review. PubMed PMID: 15591883 www.ncbi.nlm.nih.gov
- Dietert RR. Maternal and childhood asthma: risk factors, interactions, and ramifications. Reprod Toxicol. 2011 Sep;32(2):198-204. doi: 10.1016/j.reprotox.2011.04.007 Epub 2011 May 6. Review. PubMed PMID: 21575714 www.ncbi.nlm.nih.gov
- Halapi, E; Bjornsdottir, US (January 2009). "Overview on the current status of asthma genetics". The clinical respiratory journal. 3 (1): 2–7. doi:10.1111/j.1752-699X.2008.00119.x PMID 20298365. www.ncbi.nlm.nih.gov
- Riedler J, Braun-Fahrländer C, Eder W, Schreuer M, et al. Exposure to farming in early life and development of asthma and allergy: a cross-sectional survey . Lancet 2001; 358: 1129-33. PubMed
- Kelly FJ, Fussell JC. Air pollution and airway disease. Clin Exp Allergy. 2011 Aug;41(8):1059-71. doi: 10.1111/j.1365 2222.2011.03776.x Epub 2011 May 30. Review. PubMed PMID: 21623970 www.ncbi.nlm.nih.gov
- Sears MR. Trends in the prevalence of asthma. Chest. 2014 Feb;145(2):219-225. doi: 10.1378/chest.13-2059 PubMed PMID: 24493506 www.ncbi.nlm.nih.gov
- Ahluwalia SK, Matsui EC. The indoor environment and its effects on childhood asthma. Curr Opin Allergy Clin Immunol. 2011 Apr;11(2):137-43. doi: 10.1097/ACI.0b013e3283445921 Review. PubMed PMID: 21301330 www.ncbi.nlm.nih.gov
- Mackay D, Haw S, Ayres JG, et al. Smoke-free legislation and hospitalizations for childhood asthma. N Engl J Med 2010; 363: 1139-45. New England Journal of Medicine
- Mutius E, Vercelli D. Farm living: effects on childhood asthma and allergy. Nat Rev Immunol. 2010 Dec;10(12):861-8. doi: 10.1038/nri2871. Epub 2010 Nov 9. Review. PubMed PMID: 21060319 www.ncbi.nlm.nih.gov
- Lau S, Illi S, Sommerfeld C, Niggeman B, et al. Early exposure to house dust mite and cat allergens and development of childhood asthma: a cohort study. Lancet 2000; 356: 1392-7. PubMed
- Illi S, von Mutius E, Lau S, Bergmann R, Niggemann B, Sommerfeld C, Wahn U. Early childhood infectious diseases and the development of asthma up to school age: a birth cohort study. BMJ 2001; 322: 390-5. PubMed
- Johnston SL, Pattemore PK, Sanderson G, Smith S, Lampe F, Josephs L, Symington P, O'Toole S, Myint SH, Tyrrell DA, et al. Community study of role of viral infections in exacerbations of asthma in 9-11 year old children. BMJ. 1995 May 13;310(6989):1225-9. PubMed PMID: 7767192 www.ncbi.nlm.nih.gov
- Beuther DA. Obesity and asthma. Clin Chest Med. 2009 Sep;30(3):479-88, viii. doi: 10.1016/j.ccm.2009.05.002Review. PubMed PMID:19700046 www.ncbi.nlm.nih.gov
- van der Hulst AE, Klip H, Brand PL. Risk of developing asthma in young children with atopic eczema: A systematic review. J Allergy Clin Immunol 2007; 120: 565-9. PubMed
- Bergmann RL, Edenharter G, Bergmann KE, Forster J, Bauer CP, Wahn V, et al. Atopic dermatitis in early infancy predicts allergic airway disease at 5 years. Clin Exp Allergy 1998; 28: 965-70. PubMed
- Russell G, Ninan TK. Respiratory symptoms and atopy in Aberdeen school children: evidence from two surveys 25 years apart. BMJ 1992; 304: 873-5. PubMed
- Goksör E, Loid P, Alm B, et al. The allergic march comprises the coexistence of related patterns of allergic disease not just the progressive development of one disease. Acta Paediatr 2016 Dec; 105(12): 1472-1479. pmid:27381249 PubMed
- Etminan M, Sadatsafavi M, Jafari S, et al. Acetaminophen use and the risk of asthma in children and adults: a sytematic review and metaanalysis. Chest 2009; 136: 1316-23. PubMed
- Lowe AJ, Carlin JB, Bennett CM, et al. Paracetamol use in early life and asthma: prospective birth cohort study. BMJ 2010; 341: c4616. BMJ (DOI)
- Warner JO, ETAC Study Group. Early treatment of the atopic child. A double-blinded, randomized, placebo-controlled trial of cetirizine in preventing the onset of asthma in children with atopic dermatitis: 18 months' treatment and 18 months' posttreatment follow-up. J Allergy Clin Immunol 2001; 108: 929-37. PubMed
- Örtqvist AK, Lundholm C, Kieler H, et al. Antibiotics in fetal and early life and subsequent childhood asthma: nationwide population based study with sibling analysis. BMJ 2014; 349: g6979. dx.doi.org
- Hershenson MB. Rhinovirus-Induced Exacerbations of Asthma and COPD. Scientifica (Cairo). 2013;2013:405876. doi: 10.1155/2013/405876 Epub 2013 Feb 21. Review. PubMed PMID: 24278777 PMID:24278777 www.ncbi.nlm.nih.gov
- Kemp JP, Kemp JA. Management of asthma in children. Am Fam Physician 2001; 63:1341-8, 1353-4. pubmed.ncbi.nlm.nih.gov
- Global Initiative for Asthma. Pocket Guide for Asthma Management and Prevention. Stand 2022. ginasthma.org
- Leach CL, Colice GL. A pilot study to assess lung deposition of HFA-beclomethasone and CFC-beclomethasone from a pressurized metered dose inhaler with and without add-on spacers and using varying breathhold times. J Aerosol Med Pulm Drug Deliv. 2010 Dec;23(6):355-61. doi: 10.1089/jamp.2009.0783 Epub 2010 Jun 24. PubMed PMID: 20575669 www.ncbi.nlm.nih.gov
- Courtney AU, McCarter DF, Pollart SM. Childhood asthma: Treatment update. Am Fam Physician 2005; 71: 1959-68. PubMed
- Rowe BH, Spooner C, Ducharme FM, Bretzlaff JA, Bota GW. Early emergency department treatment of acute asthma with systemic corticosteroids (Cochrane review). Cochrane Database Syst Rev 2004; (4): CD002178. Cochrane (DOI)
- Powell C, Kolamunnage-Dona R, Lowe J, et al. MAGNEsium Trial In Children (MAGNETIC): a randomised, placebo-controlled trial and economic evaluation of nebulised magnesium sulphate in acute severe asthma in children. Health Technol Assess 2013; 17: 1-216. doi:10.3310/hta17450 DOI
- Mintz M. Asthma updage: Part II. Medical management. Am Fam Physicians 2004; 70: 1061-6. www.ncbi.nlm.nih.gov
- National Asthma Education and Prevention Program. Expert panel report. Guidelines for the diagnosis and management of asthma: update on selected topics, 2002. Bethesda, Md.: U.S. Department of Health and Human Services, Public Health Service, National Institutes of Health, National Heart, Lung, and Blood Institute, 2003; NIH publication no. 02-5074. www.ncbi.nlm.nih.gov
- Kelly HW, Sternberg AL, Lescher R, et al. Effect of inhaled glucocorticoids in childhood on adult height. N Engl J Med 2012; 367: 904-12. New England Journal of Medicine
- Zhang L, Prietsch SOM, Ducharme FM. Inhaled corticosteroids in children with persistent asthma: effects on growth. Cochrane Database of Systematic Reviews 2014, Issue 7. Art. No.: CD009471. DOI: 10.1002/14651858.CD009471.pub2. DOI
- Turner S, Richardson K, Murray C, Thomas M, Hillyer EV, Burden A, Price DB; Respiratory Effectiveness Group. Long- Acting β-Agonist in Combination or Separate Inhaler as Step-Up Therapy for Children with Uncontrolled Asthma Receiving Inhaled Corticosteroids. J Allergy Clin Immunol Pract. 2017 Jan - Feb;5(1):99-106.e3. doi: 10.1016/j.jaip.2016.06.009 Epub 2016 Jul 13. PubMed PMID: 27421902. www.ncbi.nlm.nih.gov
- Busse WW, Bateman ED, Caplan AL, et al. Combined Analysis of Asthma Safety Trials of Long-Acting β2-Agonists. N Engl J Med 2018; 378(26): 2497-2505. pmid:29949492 www.nejm.org
- Chauhan BF, Ben Salah R, Ducharme FM. Addition of anti-leukotriene agents to inhaled corticosteroids in children with persistent asthma. Cochrane Database Syst Rev 2013 Oct 2;10:CD009585. Cochrane (DOI)
- Robertson CF, Price D, Henry R, et al. Short-course montelukast for intermittent asthma in children: a randomized controlled trial. Am J Respir Crit Care Med 2007; 175: 323-9. PubMed
- Chauhan BF, Jeyaraman MM, Singh Mann A, Lys J, Abou-Setta AM, Zarychanski R, Ducharme FM. Addition of anti leukotriene agents to inhaled corticosteroids for adults and adolescents with persistent asthma. Cochrane Database Syst Rev. 2017 Mar 16;3:CD010347. doi: 10.1002/14651858.CD010347.pub2. Review. PubMed PMID: 28301050 www.ncbi.nlm.nih.gov
- Castro-Rodriguez JA, Rodrigo GJ. The role of inhaled corticosteroids and montelukast in children with mild-moderate asthma: results of a systematic review with meta-analysis. Arch Dis Child 2010; 95: 365-70. PubMed
- Busse WW, Morgan WJ, Gergen PJ, et al. Randomized trial of omalizumab (Anti-IgE) for astma in inner-city children. N Engl J Med 2011; 364: 1005-15. New England Journal of Medicine
- Farne HA, Wilson A, Powell C, Bax L, Milan SJ. Anti-IL5 therapies for asthma. Cochrane Database of Systematic Reviews 2017; Issue 9. Art: No.: CD010834. pmid:10.1002/14651858.CD010834.pub3 Cochrane (DOI)
- Pifferi M, Baldini G, Marrazzini G, Baldini M, Ragazzo V, Pietrobelli A, et al. Benefits of immunotherapy with a standardized Dermatophagoides pteronyssinus extract in asthmatic children: a three-year prospective study. Allergy 2002; 57: 785-90. PubMed
- Mener DJ, Lin SY. Improvement and prevention of asthma with concomitant treatment of allergic rhinitis and allergen-specific therapy. Int Forum Allergy Rhinol 2015; 5 Suppl 1: 45-50. pmid:26072703 PubMed
- Moller C, Dreborg S, Ferdousi HA, Halken S, Host A, Jacobsen L, et al. Pollen immunotherapy reduces the development of asthma in children with seasonal rhinoconjunctivitis (the PAT-study). J Allergy Clin Immunol 2002; 109: 251-6. PubMed
- Wolf FM, Guevara JP, Grum CM, Clark NM, Cates CJ. Educational interventions for asthma in children (Cochrane review). Cochrane Database Syst Rev 2004;(4):CD000326. Cochrane (DOI)
- Woodcock A, Forster L, Matthews E, Martin J, Letley L, Vickers M, et al. Control of exposure to mite allergen and allergen-impermeable bed covers for adults with asthma. N Engl J Med 2003; 349: 225-36. New England Journal of Medicine
- Kilburn S, Lasserson TJ, McKean M. Pet allergen control measures for allergic asthma in children and adults (Cochrane review). Cochrane Database Syst Rev 2004; (4): CD002989. Cochrane (DOI)
- Murray CS, Foden P, Sumner H, et al. Preventing Severe Asthma Exacerbations in Children. A Randomized Trial of Mite-Impermeable Bedcovers. Am J Respir Crit Care Med 2017; 196: 150-8. pmid:28282501 PubMed
- Lehrer PM, Vaschillo E, Vaschillo B, Lu SE, Scardella A, Siddique M, Habib RH. Biofeedback treatment for asthma. Chest. 2004 Aug;126(2):352-61. PubMed PMID:15302717 www.ncbi.nlm.nih.gov
- Eichenberger PA, Diener SN, Kofmehl R, et al. Effects of exercise training on airway hyperreactivity in asthma: a systematic review and meta-analysis. Sports Med. 2013 ;43(11):1157-70. doi: 10.1007/s40279-013-0077-2. www.ncbi.nlm.nih.gov
- Stordal K, Johannesdottir GB, Bentsen BS, et al. Acid suppression does not change respiratory symptoms in children with asthma and gastro-oesophageal reflux disease. Arch Dis Child 2005; 90: 956-60. PubMed
- Holbrook JT, Wise RA, Gold BD, et al. Lanzoprazole for children with poorly controlled asthma. JAMA 2012; 307: 373-80. www.ncbi.nlm.nih.gov
- Ahnert J, Löffler S, Müller J, Vogel H. [Systematic literature review on interventions in rehabilitation for children and adolescents with asthma bronchiale]. Rehabilitation (Stuttg). 2010 Jun;49(3):147-59. doi:10.1055/s-0030-1254081. Epub 2010 Jun 8. Review. German. PubMed PMID: 20533145 www.ncbi.nlm.nih.gov
- Beggs S, Foong YC, Le HC, Noor D, Wood-Baker R, Walters JA. Swimming training for asthma in children and adolescents aged 18 years and under. Cochrane Database Syst Rev. 2013 Apr 30;(4):CD009607. doi: 10.1002/14651858.CD009607.pub2 Review. PubMed PMID: 23633375 www.ncbi.nlm.nih.gov
- Abramson MJ, Puy RM, Weiner JM. Injection allergen immunotherapy for asthma. Cochrane Database of Systematic Reviews 2010, Issue 8. Art. No.: CD001186. pubmed.ncbi.nlm.nih.gov
- Jacobsen L, Niggemann B, Dreborg S, Ferdousi HA, Halken S, Høst A, Koivikko A, Norberg LA, Valovirta E, Wahn U, Möller C; (The PAT investigator group). Specific immunotherapy has long-term preventive effect of seasonal and perennial asthma: 10-year follow-up on the PAT study. Allergy. 2007 Aug;62(8):943-8. PubMed PMID: 17620073. www.ncbi.nlm.nih.gov
- Sannarangappa V, Jalleh R . Inhaled Corticosteroids and Secondary Adrenal Insufficiency. The Open Respiratory Medicine Journal 2014; 8: 93-100. www.ncbi.nlm.nih.gov
- Kjellman B, Gustafsson PM. Children with asthma followed up for 21 years; severity improved, but patients seldom grow out of asthma by adulthood. Läkartidningen 2000; 97: 4572-7. www.ncbi.nlm.nih.gov
- Lange P, Çolak Y, Ingebrigtsen TS, Vestbo J, Marott JL. Long term prognosis of asthma, chronic obstructive pulmonary disease, and asthma-chronic obstructive pulmonary disease overlap in the Copenhagen City Heart study: a prospective population-based analysis. Lancet Respir Med. 2016 Jun;4(6):454-62. doi: 10.1016/S2213-2600(16)00098-9 Epub 2016 Apr 6. PubMed PMID: 27061878 www.ncbi.nlm.nih.gov
- Horak E, Lanigan A, Roberts A, et al. Longitudinal study of childhood wheezy bronchitis and asthma: outcome at age 42. BMJ 2003; 326: 422-3. PubMed
- Moorman JE, Akinbami LJ, Bailey CM, Zahran HS, King ME, Johnson CA, Liu X. National surveillance of asthma: United States, 2001-2010. Vital Health Stat 3. 2012 Nov;(35):1-58. PubMed PMID: 24252609 www.ncbi.nlm.nih.gov
- Rodrigo GJ, Castro-Rodriguez JA. Anticholinergics in the treatment of children and adults with acute asthma: a systematic review with meta-analysis. Thorax 2005; 60: 740-6. PubMed
- Vézina K, Chauhan BF, Ducharme FM. Inhaled anticholinergics and short-acting beta(2)-agonists versus short-acting beta2-agonists alone for children with acute asthma in hospital. Cochrane Database Syst Rev. 2014 Jul 31 (7):CD010283. doi: 10.1002/14651858.CD010283.pub2 Review. PubMed PMID: 25080126 www.ncbi.nlm.nih.gov
- Guevara JP, Wolf FM, Grum CM, Clark NM. Effects of educational interventions for self management of asthma in children and adolescents: systematic review and meta-analysis. BMJ 2003; 326: 1308-9. pubmed.ncbi.nlm.nih.gov
Autor*innen
- Lino Witte, Dr. med., Arzt in Weiterbildung Allgemeinmedizin, Münster