Informacje ogólne
Definicja
padaczka
- Grupa chorób mózgu z trwałą predyspozycją do nagłego i niespodziewanego wystąpienia napadów padaczkowych oraz wynikających z nich konsekwencji neurobiologicznych, poznawczych, psychologicznych i społecznych.
- Do postawienia diagnozy wymagany jest co najmniej jeden napad.
- Diagnozę można postawić już po pierwszym napadzie w następujących przypadkach:
- prawdopodobieństwo wystąpienia kolejnych napadów w ciągu najbliższych 10 lat >60%
- obecność określonego - np. genetycznego - zespołu padaczkowego
Napad padaczkowy
- Napadowa zmiana świadomości, psychiki, funkcji motorycznych, percepcji autonomicznej lub czuciowej, spowodowana wyładowaniem neuronów ośrodkowych.
- EEG wykazuje pewne cechy, a mianowicie nadmierny wzrost częstotliwości i nieprawidłową synchronizację elektrycznej aktywności mózgu.
- Wzorzec napadu jest zwykle stereotypowy u osób dotkniętych chorobą, ale różni się w zależności od osoby.
Napady ogniskowe - z zaburzeniami świadomości lub bez1
- Z zaburzeniami ruchowymi na początku napadu
- automatyzmy
- napady atoniczne
- napady kloniczne
- kurcze padaczkowe
- napady hiperkinetyczne
- napady miokloniczne
- napady toniczne
- Z zaburzeniami niemotorycznymi na początku napadu
- napady autonomiczne
- napady bezruchu
- napady poznawcze
- napady emocjonalne
- napady czuciowe
- Z przejściem do obustronnych napadów toniczno-klonicznych
- Z niejasnym początkiem
- ruchowe
- toniczno-kloniczne
- kurcze padaczkowe
- nieruchowe
- bezruch
- ruchowe
- Nieklasyfikowalne
Napady uogólnione1
- Cechy wspólne
- Napady pierwotnie uogólnione nie są związane z ogniskowym początkiem lub aurą.
- Często występują zaburzenia świadomości.
- Z zaburzeniami motorycznymi
- napady toniczno-kloniczne
- napady kloniczne
- napady toniczne
- napady miokloniczne
- napady miokloniczno-toniczno-kloniczne
- napady miokloniczno-atoniczne
- napady atoniczne
- kurcze padaczkowe
- Z zaburzeniami niemotorycznymi
- typowe napady nieświadomości
- atypowe napady nieświadomości
- miokloniczne napady nieświadomości
- napady nieświadomości z miokloniami powiek
Częstość występowania
- 5% wszystkich dzieci ma napady mózgowe w dzieciństwie, a 3% wszystkich ludzi ma jeden napad w ciągu życia, często w pierwszej dekadzie.
- Są to zazwyczaj napady jednorazowe, takie jak drgawki gorączkowe lub inne napady objawowe w wyniku ostrej choroby.
- Zapadalność na napady u dzieci 60–90/100 000 rocznie
- Najwyższa zapadalność w 1. roku życia: 202/100 000 rocznie
- Chorobowość: 3–7/1000
- 59% padaczek ogniskowych, 29% padaczek uogólnionych
- Ryzyko wystąpienia padaczki jest najwyższe w 1. roku życia.
Etiologia i patogeneza
- Etiologia wieloczynnikowa
- Powszechny podział na „genetyczne“, „strukturalno-metaboliczne“ i „niejasne“ tylko częściowo odzwierciedla etiologię; często występuje połączenie przyczyn egzogennych, endogennych i genetycznych.
- Genetyka
- monogenowe lub spowodowane przez kilka czynników genetycznych
- często identyfikowane aberracje chromosomowe
- zespół mikrodelecji 15q13.3
- zespół delecji 18q
- duplikacja/inwersja chromosomu 15 (INV-DUP (15)) lub izodicentryczny chromosom 15 (IDIC (15))
- delecja 1p36
- zespół Angelmana
- zespół Downa (trisomia 21)
- zespół Klinefeltera (XXY)
- zespół Millera-Diekera (DEL 17p)
- zespół Pallistera-Killiana (częściowa tetrasomia 12p)
- zespół chromosomu pierścieniowego 14-(r14)
- zespół chromosomu pierścieniowego 20-(r20)
- trisomia 12p
- zespół Wolfa-Hirschhorna (DEL 4p)
- specyficzne mutacje, np.
- mutacje KCNQ2 i KCNQ3 u ok. 40% dzieci dotkniętych drgawkami noworodkowymi
- defekty KCNT1 u około połowy wszystkich pacjentów dotkniętych złośliwymi napadami częściowymi wędrującymi w okresie niemowlęcym
- Strukturalne
- urazy
- guzy mózgu
- zespoły nerwowo-skórne
- nadciśnienie tętnicze i choroby naczyniowe
- wady rozwojowe ośrodkowego układu nerwowego
- zaburzenia rozwojowe OUN
- po niedotlenieniu, krwotoku mózgowym, zakażeniu
- Metaboliczne
- hipo- i hiperglikemia
- niedotlenienie i zamartwica
- zapalenie opon mózgowo-rdzeniowych oraz zapalenie opon mózgowo-rdzeniowych i mózgu
- gorączką
- mocznica
- hipo- i hipernatremia
- hipokalcemia
- fenyloketonuria (PKU)
- Niejasne
Patomechanizm
- Napadowe wyładowanie neuronów z nadmiernie zwiększoną częstotliwością i nieprawidłową synchronizacją
- Objawy kliniczne zależą od lokalizacji i zakresu dysfunkcji (miejscowe vs. uogólnione).
Czynniki predysponujące
- Napady padaczkowe występują częściej u młodszych dzieci. Mózg jest niedojrzały, szybko się rozwija i ma niższy próg drgawkowy.
- Choroby przebiegające z gorączką obniżają próg drgawkowy.
- Indywidualne czynniki wyzwalające napady (brak snu, alkohol, migoczące światło)
ICD-10
- G40 Padaczka
- G40.0 Padaczka samoistna (ogniskowa) (częściowa) i zespoły padaczkowe z napadami o zlokalizowanym początku
- G40.1 Padaczka objawowa (ogniskowa) (częściowa) i zespoły padaczkowe z prostymi napadami częściowymi
- G40.2 Padaczka objawowa (ogniskowa) (częściowa) i zespoły padaczkowe ze złożonymi napadami częściowymi
- G40.3 Uogólniona samoistna padaczka i zespoły padaczkowe
- G40.4 Inne postacie uogólnionej padaczki i zespołów padaczkowych
- G40.5 Szczególne zespoły padaczkowe
- G40.6 Napady „grand mal”, nieokreślone (z napadami „petit mal” lub bez takich napadów)
- G40.7 Napady „petit mal”, nieokreślone, bez napadów „grand mal”
- G40.8 Inne padaczki
- G40.9 Padaczka, nieokreślona
- G41 Stan padaczkowy
- G41.0 Stan padaczkowy typu „grand mal”
- G41.1 Stan padaczkowy typu „petit mal”
- G41.2 Złożony częściowy stan padaczkowy
- G41.8 Inne stany padaczkowe
- G41.9 Stan padaczkowy, nieokreślony
Napady niezależne od wieku
Napady pourazowe,
- Napad wczesny/natychmiastowy
- bezpośrednio po zdarzeniu
- rzadkie
- Etiologia niejasna, napad może być nawet przyczyną urazu.
- dobre rokowanie, brak zwiększonego ryzyka padaczki
- diagnostyka różnicowa: omdlenia z objawami niedotlenienia pnia mózgu
- Wczesny napad
- 5–7 dni po zdarzeniu, u 60% w ciągu 24 godzin po urazie (wskazanie do monitorowania niemowląt po urazie głowy)
- w większości ogniskowe, w 1/3 uogólnione
- ryzyko rozwoju padaczki pourazowej 20–30%, zwykle w ciągu 2 lat od zdarzenia
- Padaczka pourazowa
- po ustąpieniu ostrych objawów
Stan padaczkowy (Status epilepticus),
- Definicja
- napad toniczno-kloniczny >5 min lub napad ogniskowy z zaburzeniami świadomości >10 min, przypadek szczególny padaczka z napadami nieświadomości >10–15 min
- Etiologia
- 26% ostra patologia (krwotok, zakażenie)
- 33% dłużej istniejące uszkodzenie/malformacje
- 22% stany gorączkowe (drgawki gorączkowe >30 min)
- 15% niejasne
- Diagnostyka/przyczyna
- 6% zaburzenia równowagi elektrolitowej
- 32% zbyt niski poziom leków przeciwpadaczkowych w surowicy
- 3,6% intoksykacje
- 4,2% wrodzone zaburzenia metaboliczne
- 43% typowe dla padaczki potencjały w EEG
- 8% obrazowanie patologii
- Powikłania
- Długotrwałe uszkodzenie należy zakładać w przypadku napadów trwających >30 minut w przypadku napadów toniczno-klonicznych i >60 minut w przypadku napadów ogniskowych.
Noworodki
Drgawki noworodkowe
- 0,5‰ wszystkich dzieci urodzonych o czasie ma drgawki w ciągu pierwszych 4 tygodni życia.
- Głównie z powodu organicznych przyczyn mózgowych (niedotlenienie, krwotok, zawał, zakażenie, wady rozwojowe itp.), diagnostyka różnicowa: zaburzenia równowagi wodno-elektrolitowej
- Objawy
- niejednorodne i czasami bardzo dyskretne objawy napadowe ze zbaczaniem gałek ocznych, oczopląsem, miokloniami powiek, nagłymi zmianami napięcia mięśniowego, bezdechem itp.
- EEG u młodszych dzieci jest mniej zróżnicowane, klasyczne potencjały typowe dla padaczki mogą być nieobecne.
- niezbędna diagnostyka poligraficzna EEG (wspomagana wideo)
- Przebieg i rokowanie
- Śmiertelność 20–30% w przypadku objawowych drgawek noworodkowych, pozostałości neurologiczne u 40%, padaczka rozwija się u 25% z organicznym pochodzeniem mózgu.
Łagodne rodzinne drgawki noworodkowe
- Dziedziczenie autosomalne dominujące, penetracja ok. 85 %
- Wykrywanie różnych molekularnych wad genetycznych w kanałach potasowych i jonowych
- Objawy
- napady kloniczne lub toniczne ze zmianami w EEG lub bez nich u dzieci urodzonych o czasie
- Przebieg i rokowanie
- zazwyczaj samoistna remisja w ciągu 1–6 tygodni
- U 15% występują później kolejne napady drgawek.
Łagodne idiopatyczne, nierodzinne drgawki noworodkowe
- 4–20% wszystkich drgawek noworodkowych
- Objawy
- napady zawsze ogniskowe lub wieloogniskowe kloniczne, czasami jako stan
- występowanie między 4. a 6. dniem życia u dzieci urodzonych o czasie.
- Chłopcy chorują częściej niż dziewczynki.
- Przebieg i rokowanie
- samoistna remisja w ciągu kilku dni
- zwiększone ryzyko wystąpienia kolejnych typów napadów i opóźnienia rozwoju w przebiegu choroby
Niemowlęta
Zespół Westa (napady zgięciowe)
- 8% wszystkich padaczek dziecięcych, zapadalność 24–42 przypadków na 100 000 urodzeń, większa częstość występowania u dzieci z zespołem Downa
- 2.–8. miesiąc życia, chłopcy chorują częściej niż dziewczynki.
- O wieloczynnikowym pochodzeniu, głównie z powodu uszkodzenia mózgu, w chorobach neurometabolicznych (w 7% związany ze stwardnieniem guzowatym )
- Objawy
- zbaczanie gałek ocznych, kiwanie głową, ruch zgięciowy tułowia i ramion (dziecko opuszcza głowę, tułów i biodra, ramiona są wyciągnięte do przodu).
- Występuje seriami, często podczas zasypiania i jedzenia.
- znaczne opóźnienie rozwoju u 90%
- EEG
- typowa hipsarytmia: utrzymująca się sekwencja nieregularnie wysokich, powolnych fal delta z desynchronicznie przeplatającymi się skokami i/lub falami ostrymi
- Przebieg i rokowanie
- śmiertelność do 3. roku życia 30%
- Rokowanie zależy od uszkodzenia mózgu.
- częsty rozwój innych padaczek, takich jak zespół Lennoxa-Gastauta (u 50%)
Zespół Ohtahary
- Poważne strukturalne uszkodzenie mózgu, związek z wadami genetycznymi STXBP1 i PLC-Beta1
- Charakterystyczne napady toniczne
- Ciągły wzorzec tłumienia impulsów w EEG zarówno podczas czuwania, jak i podczas snu
Dzieci w wieku od 6 miesięcy
Drgawki gorączkowe
- Dzieci w wieku od 6 miesięcy do 5 lat, chłopcy chorują częściej niż dziewczynki.
- Łączna częstość występowania do 5. roku życia około 3%.
- Rodzinne występowanie w 20–25% przypadków
- Proste drgawki gorączkowe: <15 min, 1 x w ciągu 24 h, uogólnione drgawki toniczno-kloniczne, w pozostałych przypadkach powikłane drgawki gorączkowe>
- Drgawki gorączkowe nie powinny być diagnozowane w przypadku infekcji OUN.
- Objawy
- przy szybko rosnącej gorączce
- najczęściej uogólnione toniczno-kloniczne
- czas trwania 10 minut
- w pojedynczych przypadkach 30–60 min zmęczenia ponapadowego
- ew. porażenie Todda po przedłużających się napadach
- Przebieg i rokowanie
- Ryzyko nawrotu istnieje przez cały czas trwania infekcji i zazwyczaj do około 5. roku życia, po czym następuje samoistna remisja.
- ryzyko wystąpienia padaczki do 7. roku życia u 3–4%
- Dzieci osób dotkniętych tą chorobą mają zwiększone ryzyko wystąpienia drgawek gorączkowych (9%) i innych postaci napadów (22%).
Padaczki z napadami nieświadomości,
- Odsetek 10–12% wszystkich padaczek dziecięcych
- Predyspozycje genetyczne, w 25% przypadków pierwotne napady uogólnione w rodzinie
- Występują u dzieci odpowiednio rozwiniętych pod względem poznawczym w wieku 2–15 lat, rzadziej wraz z wiekiem i w okresie niemowlęcym.
- Postaci
- napady nieświadomości we wczesnym dzieciństwie
- 2.–4. rok życia, głównie u chłopców
- występowanie z napadami typu grand mal lub miokloniczno-astatycznymi lub w postaci samych napadów nieświadomości
- lekkie opóźnienie w rozwoju
- rokowanie mniej korzystne niż u starszych dzieci, tendencja do nawrotów, ryzyko obniżenia sprawności poznawczej
- padaczka z napadami nieświadomości w wieku szkolnym (piknolepsja)
- głównie u dziewczynek w wieku 5–8 lat o rozwoju odpowiednim do wieku
- >100 napadów dziennie
- korzystne rokowanie przy odpowiedniej terapii, utrzymywanie się do wieku dorosłego u 1/3 i rozwój do padaczki typu grand mal u 1/3
- młodzieńcza padaczka z napadami nieświadomości
- 9.–15. rok życia, równie często u chłopców i dziewcząt, najczęściej rozwija się w zależności od wieku
- wysokie ryzyko wystąpienia napadów typu grand mal
- krótkie napady nieświadomości, często w fazie czuwania, czasami z miokloniami
- rokowanie raczej niekorzystne z tendencją do częstych napadów typu grand mal
- Objawy
- głównie napady uogólnione
- Napady nieświadomości mogą występować często i zwykle trwają 5–15 sekund.
- U 50% dzieci epizody nieświadomości są związane z łagodnymi komponentami klonicznymi, takimi jak mruganie lub łagodnymi komponentami atonicznymi, takimi jak kiwanie głową.
- W 50–80% przypadków uogólnione napady toniczno-kloniczne występują również po przebudzeniu.
- Dzieci wykazują niestabilność wegetatywną i psychiczną, mają tendencję do bólów głowy, migren, wymiotów, łatwo się niepokoją i mają skrócony czas koncentracji uwagi, czasami dyskalkulię lub inne częściowe zaburzenia funkcjonowania.
- EEG
- Wykazuje wyładowania zespołów iglica–fala wolna o częstotliwości 3 Hz z poza tym niewyróżniającą się aktywnością tła.
- Przebieg i rokowanie
- W okresie dojrzewania 15% przypadków przechodzi w padaczkę miokloniczną.
- Padaczka może wiązać się z upośledzeniem funkcji poznawczych i/lub zaburzeniami uczenia się.
- Padaczka prawie zawsze ustępuje samoistnie.
- W badaniach z krótką obserwacją (5–8 lat) wskaźnik remisji wynosi 78%, ale liczba remisji zmniejsza się wraz z długością obserwacji. W wieku dorosłym 25–40% pacjentów ma padaczkę z uogólnionymi napadami toniczno-klonicznymi.
Zespół Lennoxa-Gastauta
- Rzadka postać padaczki, początek w wieku przedszkolnym (2–7 lat)
- 3–5% wszystkich padaczek dziecięcych
- Chłopcy chorują częściej niż dziewczynki, głównie dzieci z uszkodzeniami mózgu (dysgenezja, stwardnienie guzowate, choroby neurometaboliczne) z upośledzeniem umysłowym w >90% przypadków.
- Poprzedzający zespół Westa w 20% przypadków
- Objawy
- niejednorodne typy napadów (głównie asymetryczne, toniczne (upadki toniczne), astatyczne, miokloniczne, ogniskowe, toniczno-kloniczne, atypowe napady nieświadomości lub złożone napady częściowe), głównie drobne napady uogólnione, serie napadów z bardzo dyskretnymi objawami w nocy, upadki toniczne w ciągu dnia
- EEG
- Wykazuje patologicznie powolną aktywność tła i powolną uogólnioną aktywność epileptyczną (<3 hz).>
- Przebieg i rokowanie
- niekorzystne rokowanie, zwłaszcza w przypadku rozwoju z zespołu Westa
- w 50% przypadków kontrola napadów za pomocą leków
- Częste i długotrwałe epizody prowadzą do demencji.
Zespół Landaua-Kleffnera (afazja padaczkowa)
- Idiopatyczna padaczka częściowa, nakładająca się na padaczkę Rolanda i rzekomy zespół Lennoxa
- Wcześniej zdrowe dzieci w wieku 4–10 lat
- Chłopcy chorują częściej niż dziewczynki.
- Objawy
- częściowa lub całkowita agnozja słuchowa spowodowana zaburzeniami korowego przetwarzania sygnałów słuchowych, skutkująca dysfazją aż do afazji, zaburzenia zachowania
- napady ogniskowe lub uogólnione (jak w przypadku padaczki Rolanda)
- EEG
- wieloogniskowa aktywność padaczkowa w obszarach skroniowych bez wyraźnej dominacji bocznej
- częsta, czasami ciągła aktywność typu iglica-fala (spike-wave) w fazie głębokiego snu
- Przebieg i rokowanie
- niejednorodny przebieg od krótkich, łagodnych do długich i postępujących postaci
- tendencja do nawrotów
- często pozostałości zaburzeń mowy
Łagodna padaczka z ostrymi falami środkowo-skroniowymi (padaczka Rolanda),
- Obok padaczki z napadami nieświadomości jest to jedna z najczęstszych padaczek w dzieciństwie (8–23%)
- U dzieci rozwiniętych odpowiednio do swojego wieku od 2. do 10. roku życia, objawy zwykle między 5. a 9. rokiem życia
- Chłopcy chorują częściej niż dziewczynki.
- Przed wystąpieniem objawów w przeszłości występowały drgawki gorączkowe i drgawki noworodkowe
- Przyczyny
- genetyczne, nieznany gen, prawdopodobnie dziedziczne zaburzenie dojrzewania mózgu
- u 20-30% dodatni wywiad rodzinny w kierunku padaczki
- Objawy
- początek często z parestezjami w okolicy twarzy
- ogniskowe napady czuciowo-ruchowe w okolicy głowy, napady toniczne lub kloniczne w okolicy twarzy, zaburzenia mowy (również utrzymujące się po napadzie), możliwe zajęcie mięśni gardła i krtani, następnie zadławienie, jęki
- około 75% napadów podczas snu
- możliwe przejście we wtórnie uogólnione napady toniczno-kloniczne
- U 2/3 chorych występują głównie uogólnione napady toniczno-kloniczne.
- EEG
- ostre fale, głównie centralno-skroniowe, o zmiennej lokalizacji
- Przebieg i rokowanie
- samoistna remisja do okresu dojrzewania
- w 5% przypadków poważne napady w późniejszym przebiegu
Młodzież i młodzi dorośli
Młodzieńcza padaczka z napadami nieświadomości
Młodzieńcza padaczka miokloniczna (zespół Janza)
- Zespół idiopatycznej padaczki uogólnionej, 5–15% wszystkich padaczek
- Osoby zdrowe w wieku 12–25 lat
- Objawy
- symetryczne mioklonie obręczy barkowej, zwykle rano (objawy są czasami niezauważane i wymagają aktywnego badania; typowe: szczoteczka do zębów wypada z ręki, opisywane jako drganie, porażenie prądem lub podobne)
- czasami z napadami nieświadomości lub porannymi napadami toniczno-klonicznymi (u 80–95%, padaczka z wybudzeniem)
- związek z brakiem snu, spożyciem alkoholu, miesiączką lub stresem
- EEG
- Wykazuje niepozorną aktywność tła z przeplatającymi się uogólnionymi zespołami wieloiglicy-fali wolnej.
- Czasami (38%) aktywność typu iglica-fala jest asymetryczna, a u 10% międzynapadowy zapis EEG jest bez zmian.
- Przebieg i rokowanie
- W młodzieńczej padaczce mioklonicznej rzadko dochodzi do remisji. Często konieczne jest leczenie przez całe życie. Jednak przy odpowiedniej terapii rokowanie jest korzystne.
Diagnostyka
Kryteria diagnostyczne
- Rejestracja napadu za pomocą EEG (rzadko udana)
- Wykrycie potencjałów typowych dla padaczki w EEG
- Prawdopodobieństwo jest najwyższe 24 godziny po napadzie.
- Uwaga: 3% wszystkich dzieci ma typowe dla padaczki potencjały w spoczynkowym EEG bez obecności padaczki!
- Brak dowodów na występowanie potencjałów typowych dla padaczki nie wyklucza rozpoznania.
Diagnostyka różnicowa
Różnicowanie z zespołami padaczkowymi
- Oprócz wyżej wymienionych zespołów padaczkowych, w przypadku napadów drgawkowych u dzieci i młodzieży należy rozważyć poniższe rozpoznania różnicowe (więcej informacji na temat poszczególnych rozpoznań różnicowych można znaleźć w artykule Napady niepadaczkowe i padaczkowe u dzieci).
- Drgawki afektywne
- Omdlenia
- Mioklonie
- mioklonie senne u noworodków
- łagodne mioklonie u niemowląt
- zespół opsoklonie–mioklonie
- hiperekpleksja
- mioklonie przysenne
- Napadowe zaburzenia ruchowe
- stereotypie ruchowe związane z autostymulacją, zjawiska gratyfikacji (masturbacja dziecięca), na przykład w autyzmie lub niepełnosprawności intelektualnej
- łagodne napadowe pozycyjne zawroty głowy
- napadowy kręcz szyi
- napadowa kinezygenna choreoatetoza
- napadowa dystoniczna choreoatetoza (Mount-Reback)
- ataksje epizodyczne (EA1, EA2)
- naprzemienna hemiplegia dziecięca
- zespół Sandifera
- drżenie kiwające (spasmus nutans)
- łagodne napadowe toniczne spojrzenie w górę
- Migrena (np. migrena podstawna)
- Zespoły psychogenne
- Zjawiska związane ze snem (patrz również artykuł Parasomnie u dzieci), np.:
- lęki nocne
- narkolepsja i katapleksja
- somnambulizm
- paraliż senny
Możliwe przyczyny napadów padaczkowych
- Zapalenie opon mózgowo-rdzeniowych lub zapalenie opon mózgowo-rdzeniowych i mózgu
- Zaburzenia elektrolitowe, takie jak hipokalcemia, hipo-/hipernatremia lub hipo-/hiperglikemia
- Drgawki noworodków są często spowodowane uszkodzeniami organicznymi lub zaburzeniami metabolicznymi.
- Więcej w rozdziale Etiologia i patogeneza
Wywiad lekarski
- Szczegółowy wywiad z osobą dotkniętą chorobą, jej rodziną i, w razie potrzeby, osobami z szerszego otoczenia (szkoła, krąg znajomych itp.)
- Ogólny wywiad lekarski
- ciąża
- okres noworodkowy
- rozwój neurologiczny
- wywiad rodzinny
- leki
- wypadki/upadki
- operacje
- Wywiad dotyczący napadów (objawy niekiedy nie są rozpoznawane i należy o nie dokładnie zapytać)
Czynniki ryzyka
- Czas
- Opis
- Aura
- Subiektywne doświadczenia dziecka podczas napadu
- Sinica
- Analiza nagrań wideo
- Filmy nagrane przez rodziców również mogą być cenne.
Badanie przedmiotowe przeprowadzone przez specjalistów w dziedzinie pediatrii i/lub neurologii dziecięcej
- Pełne badanie fizykalne
- Gorączka, objawy zakażenia
- Stan neurologiczny
- Możliwe zmiany napadowe w EEG
- Porażenie poudarowe
- Znamiona syndromalne, w szczególności wskazujące na choroby nerwowo-skórne
- Hepatosplenomegalia jako wskaźnik defektu metabolicznego
- Opóźnienie rozwojowe2
Diagnostyka laboratoryjna przeprowadzona przez specjalistów w dziedzinie pediatrii, neurologii dziecięcej i, w razie potrzeby, genetyki
Pobranie próbki krwi
- Podstawowa diagnostyka noworodków i niemowląt po pierwszym napadzie
- Podstawowa diagnostyka po pierwszym napadzie padaczkowym u starszych dzieci, zwłaszcza z zaburzeniami czujności lub reaktywności w okresie ponapadowym
- Na, Ca, glukoza
- test przesiewowy na obecność narkotyków lub leków
- Oznaczanie stężenia leków przeciwpadaczkowych w osoczu
- w przypadku nawrotu po ustąpieniu napadów
- w przypadku wystąpienia działań niepożądanych, niewystarczającego działania, politerapii, innych chorób, po podaniu dawki (odczekać co najmniej 5 okresów półtrwania), zmiany dawki lub wyraźnej zmiany masy ciała
- Rejestracja narządowo swoistych działań niepożądanych leków przeciwpadaczkowych
- np. jeśli istnieje kliniczne podejrzenie zaburzeń elektrolitowych
- przed rozpoczęciem terapii i 4 tygodnie po jej zakończeniu: morfologia krwi, AST, ALT, bilirubina, amylaza, wskaźnik Quicka, PTT; powtórzyć u osób bez objawów klinicznych ale z nieprawidłowymi wartościami laboratoryjnymi: 3 razy w odstępach ≤2 tygodni, a następnie co miesiąc do miesiąca 6
- przed operacjami: oprócz wspomnianych parametrów krzepnięcia, czas krwawienia i diagnostyka zespołu Willebranda (ponieważ podejrzewa się, że leki przeciwpadaczkowe, takie jak walproinian, sprzyjają bardzo rzadkiej nabytej postaci tej choroby)
- W przypadku dzieci opóźnionych w rozwoju dodatkowo kompleksowe wykluczenie zaburzeń metabolicznych, jeśli to możliwe
- co najmniej: mleczan, gazometria, kwas moczowy, amoniak, glikemia, acylokarnityny, aminokwasy w osoczu, kwasy organiczne w moczu
- rozważenie testów genetycznych w celu wykluczenia mutacji POLG1
- Możliwe potwierdzenie rozpoznania napadu padaczkowego
- prolaktyna w ciągu 1 godziny po napadzie (w zakresie referencyjnym dla napadów nieświadomości i dysocjacyjnych, podwyższona dla napadów uogólnionych, a w niektórych przypadkach także ogniskowych, niedotlenienia i omdleń)
- podwyższony poziom kinazy kreatynowej po napadzie uogólnionym
Badanie płynu mózgowo-rdzeniowego
- W przypadku podejrzenia zapalenia OUN (np. zapalenie opon mózgowo-rdzeniowych, autoimmunologiczne zapalenie mózgu)
- W przypadku złożonych drgawek gorączkowych
- U dzieci w wieku <6 miesięcy>
Badania genetyczne
- Analiza chromosomów, klasyczne kariotypowanie, FISH, badanie całogenomowe z zastosowaniem wysokorozdzielczych mikromacierzy (SNP array), ukierunkowana diagnostyka pojedynczych genów, sekwencjonowanie następnej generacji (NGS)
- Do rozważenia, jeśli etiologia jest niejasna.
- Zwłaszcza w przypadku dodatkowego upośledzenia umysłowego, znamion syndromalnych/nieprawidłowości fenotypowych
Diagnostyka metaboliczna
- W przypadku wskazań klinicznych, np. podstawowe badania laboratoryjne
- W przypadku niejasnej etiologii
- Jeśli napady są oporne na leczenie
Diagnostyka autoimmunologiczna
- Przy odpowiednim podejrzeniu
- Przeciwciała antyneuronalne (antygeny powierzchniowe komórek neuronalnych)
- Przeciwciała onkoneuronalne (wewnątrzkomórkowe antygeny neuronalne)
- Przeciwciała niespecyficznie skierowane przeciwko strukturom neuronalnym
Diagnostyka instrumentalna
EEG
- Zapisy czuwania, zapisy snu (szczególnie ważne u dzieci), zapisy deprywacji snu/snu, zapisy długoterminowe/24-godzinne EEG, telemetria wideo/poligrafia
- Ocena przez specjalistów
- co najmniej 20 minut (60 minut dla noworodków, jeśli to możliwe), w tym hiperwentylacja i/lub fotostymulacja (metody aktywacji) i faza snu
- hiperwentylacja jest przeciwwskazana ze względu na wywołane nią zwężenie naczyń mózgowych w następujących przypadkach:
- podejrzenie chorób naczyniowo-mózgowych, w tym krwotoku śródczaszkowego lub podtwardówkowego
- niedokrwistość sierpowatokrwinkowa
- ciężka migrena
- wzrost ciśnienia wewnątrzczaszkowego
- niedawno przebyty uraz czaszkowo-mózgowy
- Rejestracja inwazyjna tylko przed planowaną operacją padaczki
- Wykrycie potencjałów typowych dla padaczki najprawdopodobniej w ciągu 24 godzin po napadzie
Diagnostyka obrazowa
- MRI
- diagnostyka 1. wyboru
- wykrywanie dysplazji, stwardnienia, wad rozwojowych itp.
- wskazanie
- we wszystkich nowo występujących padaczkach (opcjonalnie w typowej padaczce z napadami nieświadomości w wieku szkolnym i młodzieńczym, młodzieńczej padaczce mioklonicznej, padaczce Rolanda)
- w przypadku nietypowego przebiegu wymienionych zespołów padaczkowych
- w przypadku ponapadowych deficytów neurologicznych trwających kilka godzin (porażenie Todda) lub utrzymującego się upośledzenia czujności
- Należy rozważyć w przypadku zaburzeń poznawczych, ruchowych lub innych zaburzeń neurologicznych o niejasnej etiologii.
- w przypadku napadu z objawami ogniskowymi
- u dzieci w wieku <1 roku życia>
- w przypadku EEG bez objawów padaczki Rolanda lub padaczki pierwotnie uogólnionej
- w przypadku padaczki opornej na leczenie
- do kontroli progresji ze znanym ogniskiem
- do diagnostyki przedoperacyjnej
- TK
- niższa rozdzielczość niż MRI
- w stanach ostrych (może być wykonana szybko i bez sedacji)
- do wykrywania małych krwotoków i zwapnień
- USG czaszki
- Jeśli ciemiączko jest nadal otwarte, ewentualnie jako obrazowanie pierwotne, ewentualnie z rezonansem magnetycznym w późniejszym terminie.
- W razie potrzeby funkcjonalny MRI, PET lub SPECT do diagnostyki przedoperacyjnej
Wskazania do skierowania
- Skierowanie do specjalisty neuropediatrii w przypadku podejrzenia padaczki
- Leczenie stanów ostrych i hospitalizacja w przypadku status epilepticus
- Monitorowanie kliniczne w przypadku drgawek gorączkowych
Leczenie
Cele terapii
- Celem jest:
- ustąpienie napadów lub zmniejszenie częstotliwości napadów
- jeśli to możliwe, uniknięcie lub jeśli to konieczne, zaakceptowanie niewielkich skutków ubocznych
- zapobieganie powikłaniom
- umożliwienie prawidłowego rozwoju
- poprawa jakości życia
Ogólne informacje o leczeniu
- Opcje leczenia obejmują farmakoterapię, operację padaczki, neurostymulację, dietę ketogeniczną
- Brak odpowiedzi po prawidłowym zastosowaniu 2 leków przeciwpadaczkowych uznaje się za farmakooporność
- Leczenie jest zawsze indywidualne i powinno być prowadzone i monitorowane przez specjalistyczny i interdyscyplinarny zespół (neurologia rozwojowa, epileptologia dziecięca).
- Skuteczność leku musi być badana indywidualnie dla danej osoby i rodzaju padaczki.
- Konieczne jest ścisłe przestrzeganie zaleceń dotyczących przyjmowania leków.
- Często konieczne jest dostosowanie stylu życia (unikanie niedoboru snu, nieregularnego rytmu życia, alkoholu, migoczącego światła lub podobnych indywidualnych czynników, które wywołują napady).
Leczenie farmakologiczne – leki przeciwpadaczkowe
- Skuteczność leków
- kanały sodowe (karbamazepina, okskarbazepina, octan eslikarbazepiny)
- kanały wapniowe (etosuksymid, mezuksymid)
- kwas γ-aminomasłowy (tiagabina, stiripentol)
- glutaminian (perampanel)
- Uwalnianie neuroprzekaźników (lewetyracetam, brywaracetam)
- hamowanie anhydrazy węglanowej (sultiam, acetazolamid)
- mechanizmy łączone (walproinian, topiramat, zonisamid, felbamat)
- Działania niepożądane
- zawroty głowy, zaburzenia widzenia, zmęczenie (w zależności od dawki)
- zaburzenia zachowania (fenobarbital, walproinian, gabapentyna, topiramat, lewetyracetam, zonisamid)
- depresja, tendencje samobójcze, agresywność
- zaburzenia funkcji poznawczych (fenobarbital, fenytoina, topiramat, zonisamid)
- zaburzenia czynności szpiku kostnego (karbamazepina, etosuksymid, felbamat, lamotrygina, fenobarbital, fenytoina, prymidon, walproinian)
- zaburzenia czynności wątroby (karbamazepina, etosuksymid, felbamat, gabapentyna, lewetyracetam, lamotrygina, okskarbazepina, fenobarbital, fenytoina, prymidon, wigabatryna, walproinian)
- zespół Stevensa-Johnsona (lamotrygina, zwłaszcza w połączeniu z walproinianem)
- nieodwracalne wady pola widzenia (wigabatryna)
- aseptyczne opon mózgowo-rdzeniowych (lamotrygina)
- teratogenność (zwłaszcza walproinian)
- Przypuszczalne synergistyczne działanie walproinianu + lamotryginy, walproinianu + karbamazepiny, fenobarbitalu + fenytoiny, karbamazepiny + gabapentyny. Przykłady monoterapii:
- lamotrygina w napadach ogniskowych i uogólnionych od 12. roku życia i zespole Lennoxa-Gastauta od 2. roku życia, leczenie z wyboru typowych napadów nieświadomości
- lewetyracetam od 16. roku życia w przypadku napadów ogniskowych
- topiramat od 2. roku życia w leczeniu napadów ogniskowych i uogólnionych, lek przeciwpadaczkowy o szerokim spektrum działania
- Sultiam w przypadku padaczki Rolanda (jeśli terapia jest konieczna). Przykłady terapii skojarzonej (tylko jeśli monoterapia nie jest skuteczna):
- lamotrygina jako leczenie uzupełniające napadów uogólnionych i ogniskowych od 2. roku życia (+ walproinian)
- walproinian, etosuksymid i lamotrygina w skojarzeniu w napadach nieświadomości
- walproinian + lamotrygina w leczeniu zespołu Janza
Leki przeciwpadaczkowe a ciąża
- Brak ogólnych przeciwwskazań do stosowania leków przeciwpadaczkowych o potencjale teratogennym u dziewcząt w wieku rozrodczym
- Stosowanie walproinianu tylko wtedy, gdy inne leki przeciwpadaczkowe są nieskuteczne
- Jeśli to możliwe, należy unikać politerapii, ponieważ zwiększa ona ryzyko wystąpienia wad rozwojowych.
- Płodność zmniejszona nawet o 1/3 w porównaniu do zdrowych kobiet
- Stosowanie leków przeciwpadaczkowych zalecanych w celu zapobiegania niekontrolowanym napadom podczas ciąży
- Większość ciąż i porodów u kobiet z padaczką bez powikłań
- Częstotliwość napadów podczas ciąży bez zmian w 2/3, zmniejszona w 16% i zwiększona w 17% przypadków (przebieg zależny od stosowanego leku przeciwpadaczkowego).
- Ryzyko wad rozwojowych zależne od dawki lamotryginy, walproinianu, karbamazepiny
- Wskaźnik wad rozwojowych jest najwyższy w przypadku walproinianu (dawka >1500 mg, ryzyko 24,2%).
- Korzystny profil ryzyka dla lewetyracetamu (1,6%) i lamotryginy (dawka <300 mg, ryzyko 2%)>
- Zalecane spożycie 5 mg kwasu foliowego dziennie w okresie przed poczęciem do końca 1. trymestru
- Ogólnie zaleca się karmienie piersią, należy sprawdzić, czy nie występują objawy przedawkowania, w razie potrzeby sprawdzić stężenie leku w surowicy
Leki przeciwpadaczkowe i antykoncepcja hormonalna
- Korzystne są preparaty niskodawkowe (minipigułka), ponieważ generalnie nie należy zakładać wpływu na nasilenie lub częstotliwość napadów (wyjątek: lamotrygina, tutaj wzajemne zmniejszenie skuteczności działania antykoncepcyjnego i przeciwpadaczkowego, zalecane stosowanie monopreparatu progestagenowego).
- Antykoncepcja hormonalna nieskuteczna w przypadku leczenia:
- karbamazepiną
- felbamatem
- fenobarbitalem
- fenytoiną
- prymidonem
- Możliwe osłabienie skuteczności antykoncepcji hormonalnej w przypadku leczenia:
- etosuksymidem
- topiramatem
- okskarbazepiną
- lamotryginą
- Brak osłabienia skuteczności antykoncepcji hormonalnej w przypadku leczenia:
- gabapentyną
- pregabaliną
- wigabatryną
- lewetyracetamem
- kwasem walproinowym
- zonisamidem
Procedura leczenia początkowego
- Monoterapia, dawkowanie do pierwszej odpowiedniej dawki
- Jeśli cel leczenia nie zostanie osiągnięty, należy zwiększyć dawkę, odstawić lub zmienić lek.
- Jeśli cel leczenia nie zostanie osiągnięty po pierwszym zwiększeniu dawki, należy zwiększyć dawkę do maksymalnej, odstawić lub zmienić lek.
- maksymalna dawka: limit skutków ubocznych, maksymalne stężenie w surowicy w odniesieniu do długotrwałej toksyczności, najwyższa rozsądna dawka dla osiągniętej odpowiedniej masy ciała
- Połączenie z drugim lekiem przeciwdrgawkowym, jeśli początkowa terapia jest skuteczna, ale nie może być dalej zwiększana
Leczenie drgawek gorączkowych
- Diazepam doodbytniczo
- 5 mg w przypadku dzieci o masie ciała <15 kg>
- 10 mg w przypadku dzieci o masie ciała >15 kg
- w razie potrzeby 2. podanie tej samej dawki w przypadku utrzymywania się napadu
- Midazolam dopoliczkowo
- 2,5 mg u dzieci w wieku od 6 miesięcy do 1 roku
- 5 mg dla dzieci w wieku 1–5 lat
- w razie potrzeby 2. podanie tej samej dawki w przypadku utrzymywania się napadu
- Midazolam dożylnie
- 0,1–0,2 mg/kg m.c. (2 mg/min)
- Lorazepam dożylnie
- 0,05 mg/kg m.c. (2 mg/min)
- Diazepam dożylnie
- 0,25 mg/kg m.c. (5 mg/min)
Leczenie stanu padaczkowego w warunkach ambulatoryjnych
- Klonazepam dożylnie
- niemowlęta 0,01–0,07 mg/kg masy ciała
- małe dzieci i dzieci w wieku szkolnym 0,01–0,05 mg/kg m.c.
- Diazepam dożylnie
- niemowlęta 0,3–0,5 mg/kg masy ciała
- małe dzieci i dzieci w wieku szkolnym 0,2–0,4 mg/kg m.c.
- Diazepam doodbytniczo
- do ok. 15 kg masy ciała: 5 mg
- powyżej ok. 15 kg masy ciała: 10 mg
- Midazolam dopoliczkowo
- dopoliczkowo 0,2–0,5 mg/kg masy ciała (podawanie ambulatoryjne możliwe od 6 miesiąca życia; maksymalna dawka 10 mg)
- Lorazepam (niezatwierdzony do przerywania stanu)
- do ok. 20 kg masy ciała: 1 mg
- Patrz także artykuł Stan padaczkowy.
- Uporczywe napady padaczkowe lub powtarzające się napady bez powrotu do zdrowia między napadami
- Uogólnione napady toniczno-kloniczne (najczęstsze) wymagają natychmiastowego leczenia szpitalnego.
- Należy oznaczyć poziom glikemii, aby wykluczyć hipoglikemię.
- Należy zapobiegać niedrożności dróg oddechowych i samookaleczeniom.
Padaczka oporna na leczenie
- W przypadku niewystarczającej odpowiedzi na leczenie farmakologiczne, częstość napadów u dzieci i dorosłych, u których padaczka wystąpiła po raz pierwszy w dzieciństwie, można zmniejszyć, podając dodatkowo leki zawierające kannabinoidy, przy czym w wielu przypadkach występują reakcje niepożądane (Ia)3.
Operacja padaczki
- Stosowana w padaczce opornej na leczenie farmakologiczne (2 leki w dawce)
- Jest wskazana u 10–15% pacjentów z padaczką oporną na leczenie farmakologiczne.
- Ustąpienie napadów uzyskuje się w 70% przypadków.
- Korzystny wpływ na rozwój, zwłaszcza u młodszych dzieci
- Niezbędna jest kompleksowa diagnostyka przedoperacyjna:
- wywiad lekarski, semiologia
- powierzchniowe EEG
- MRI
- inwazyjne EEG
- obrazowanie czynnościowe
- testy neuropsychologiczne
- Lecznicze metody chirurgiczne
- lesionektomia i topektomia (lecznicza)
- lobektomia
- hemisferektomia
- wielokrotne przecięcia podoponowe
- Paliatywne metody chirurgiczne
- kalozotomia
- stymulacja nerwu błędnego
- wskazana w przypadkach oporności na farmakoterapię i nieudanej lub beznadziejnej operacji padaczki
- Nerw błędny jest stymulowany co 5 minut za pomocą elektrody umieszczonej w lewym nerwie błędnym.
- Częstotliwość napadów zmniejsza się o >50% w 35–60% przypadków.
- Ma działanie poprawiające nastrój, nie ma istotnych skutków ubocznych, może być stosowana równolegle z lekami przeciwpadaczkowymi.
Terapia dietą ketogeniczną
- Szczególnie skuteczna w przypadku określonych zespołów padaczkowych (patrz wyżej)
- Dieta niskowęglowodanowa, wysokotłuszczowa, zbilansowana białkowo i kalorycznie (stosunek tłuszczów do produktów beztłuszczowych = 4:1)
- Indywidualne tworzenie planu żywieniowego, rozpoczęcie w warunkach stacjonarnych
- Niejasny mechanizm działania
- Odpowiedź najwcześniej po 8 tygodniach, utrzymująca się przez co najmniej 1 rok
- Często niedostateczne przestrzeganie zaleceń w przypadku starszych dzieci i młodzieży
- Niespójne dane dotyczące wpływu tej terapii na ryzyko sercowo-naczyniowe
- >70% kontroli napadów (zalecenie terapii dietą ketogeniczną) w następujących przypadkach:
- zespół Angelmana
- zespół Dravet
- padaczka z napadami miokloniczno-atonicznymi (zespół Doose)
- zespół padaczkowy związany z zakażeniem przebiegającym z gorączką (FIRES)
- padaczki lekooporne, w tym superoporny stan padaczkowy
- jedyne wskazanie do karmienia mieszanką przez rurkę PEG
- Mitochondriopatie kompleksu 1
- Zespół Ohtahary
- zespół stwardnienia guzowatego
- zespół Westa
- Około 50% kontroli napadów (rozważenie terapii dietą ketogeniczną) w następujących przypadkach:
- napady nieświadomości
- encefalopatia padaczkowa związana z CDKL5
- ESES (padaczka z ciągłymi wyładowaniami zespołów iglica-fala we
śnie) - młodzieńcza padaczka miokloniczna
- wady rozwojowe kory mózgowej
- choroba Lafora
- zespół Landaua-Kleffnera
- Zespół Lennoxa-Gastauta
- zespół Retta
- padaczka niemowlęca z wędrującymi napadami ogniskowymi
- podostre stwardniające zapalenie mózgu (SSPE)
Przebieg, powikłania i rokowanie
Przebieg
- Duża zmienność w zależności od typu padaczki, częstotliwości i długości napadów, odpowiedzi na leczenie, chorób współistniejących, wieku
- Przy odpowiednio dobranej i wdrożonej terapii początkowej u 50% wszystkich dzieci z padaczką napady ustępują, u kolejnych 25% po podaniu drugiego leku, w 38% wszystkich pozostałych przypadków nie dochodzi do napadów przez ponad rok w trakcie trwania choroby, a nawroty napadów występują u 2/3 osób dotkniętych chorobą.
- 60% padaczek opornych na leczenie farmakologiczne można skutecznie leczyć chirurgicznie.
Powikłania
- Zaburzenia rozwojowe
- Zaburzenia poznawcze
- Współistniejące choroby psychiczne (również spowodowane przez leki)
- Skutki uboczne leków
- Często konieczne jest dostosowanie/ograniczenie codziennych nawyków.
- unikanie niedoboru snu, nieregularnego rytmu życia
- ew. rozpoczęcie przyjmowania leków podczas długich lotów
- ograniczenie spożycia kofeiny i alkoholu, unikanie wysokoprocentowych napojów alkoholowych
- niezażywanie narkotyków (w tym samym czasie często niedostateczne przestrzeganie zaleceń)
- ew. brak prawa jazdy
- kontrolowane planowanie rodziny i antykoncepcja
- ew. ograniczenie wyboru szkoły i kariery zawodowej
- ew. unikanie migoczącego światła lub podobnych indywidualnych czynników wyzwalających napady (ryzyko wyzwalania napadów przez ekrany komputerów i telewizorów wydaje się być bardzo niskie)
Rokowanie
- Bardzo zmienne rokowanie, w zależności od wieku, rodzaju padaczki, częstotliwości i długości napadów, odpowiedzi na leczenie, chorób współistniejących
Dalsze postępowanie
- Indywidualne, zwykle w ramach konsultacji pediatrycznej dotyczącej padaczki
Informacje dla pacjentów
O czym należy poinformować pacjenta?
- O chorobie i wyborze zawodu
Informacje dla pacjentów w Deximed
Ilustracje
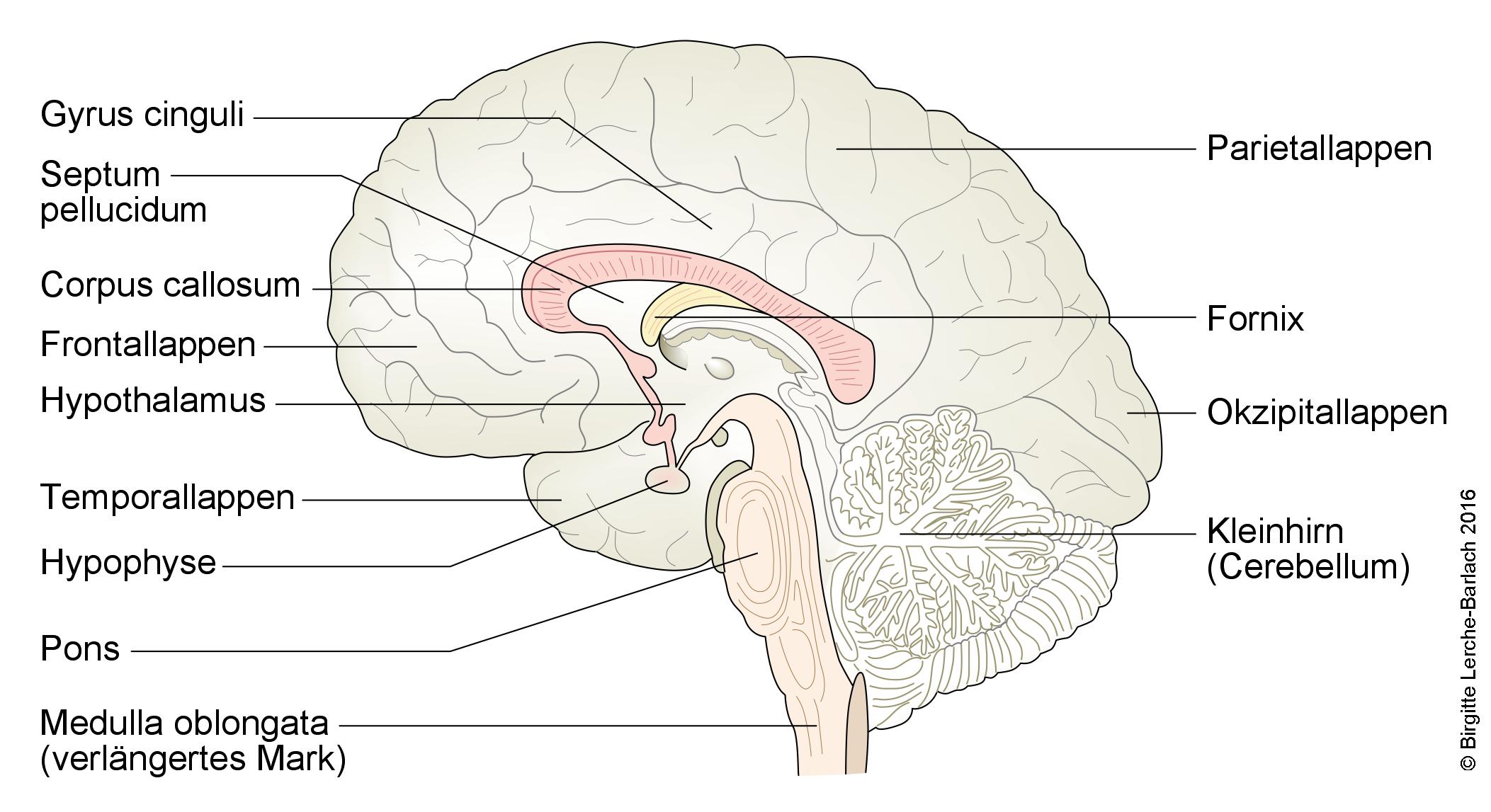
Przegląd kory mózgowej - widok środkowo-przyśrodkowy
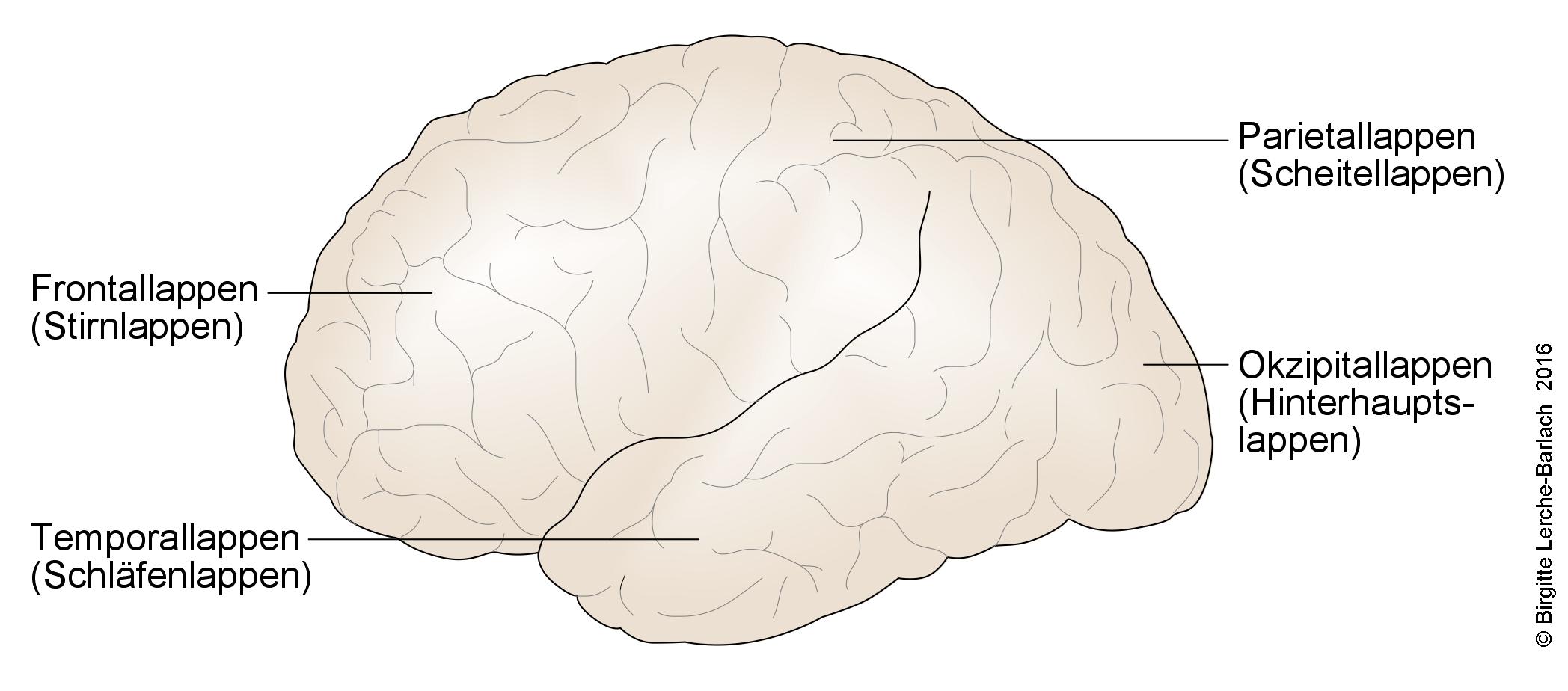
Przegląd kory mózgowej – widok z boku
Quellen
Literatur
- Fisher RS, Cross JH, French JA et al. Operational classification of seizure types by the International League Against Epilepsy: Position Paper of the ILAE Commission for Classification and Terminology. Epilepsia 2017; 58: 522-530. doi:10.1111/epi.13670 DOI
- Lopes AF, Simões MR, Monteiro JP, Fonseca MJ, Martins C, Ventosa L, et al. Intellectual functioning in children with epilepsy: Frontal lobe epilepsy, childhood absence epilepsy and benign epilepsy with centro-temporal spikes. Seizure. 2013 Aug 12. pdfs.semanticscholar.org
- Stockings E, Zagic D, Campbell G, et al. Evidence for cannabis and cannabinoids for epilepsy: a systematic review of controlled and observational evidence. J Neurol Neurosurg Psychiatry 2018 Mar 6; pii: jnnp-2017-317168: Epub ahead of print. pmid:29511052 PubMed
Autor*innen
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg
- Anne Strauß, Ärztin in Weiterbildung Pädiatrie, Zentrum für Kinder- und Jugendmedizin, Universitätsklinikum Freiburg